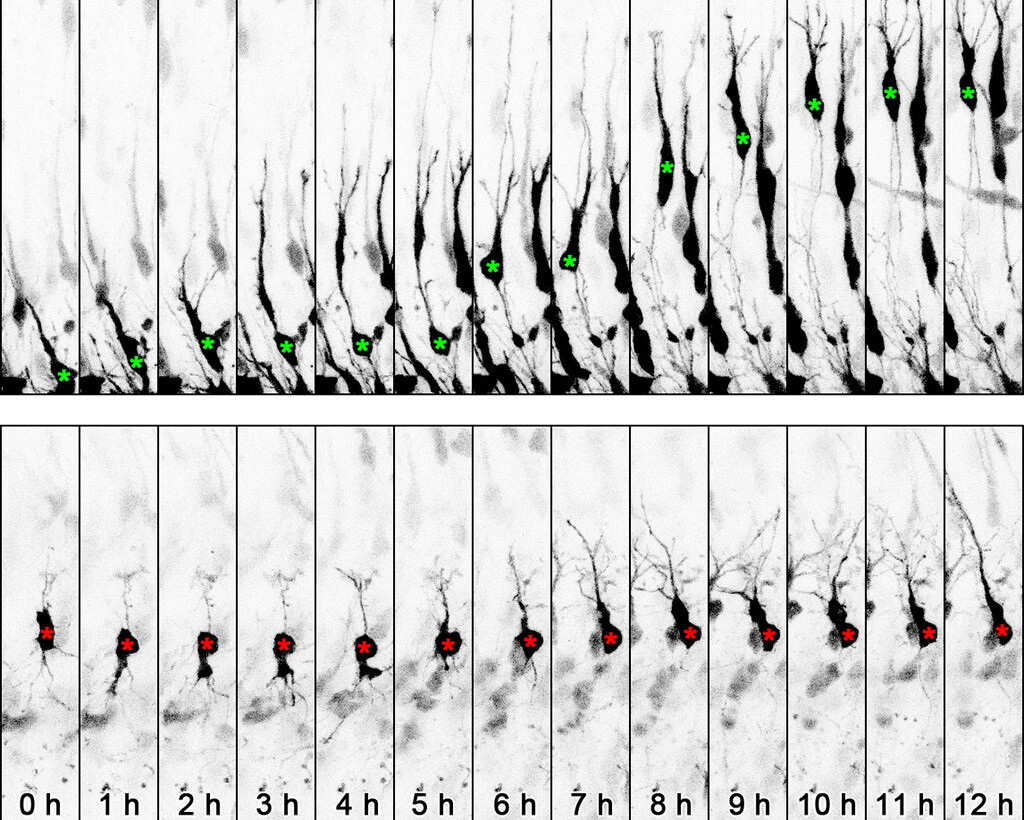
Wandernde Neuronen auf Abwegen können sich zu Irrläufern im Gehirn entwickeln. Die Wanderungsbewegungen von Nervenzellen unterliegen dabei molekularen Mechanismen.
Bei ihren Forschungen zur Gehirnentwicklung gewannen Ulmer Wissenschaftler faszinierende Einblicke in die Wanderungsbewegungen von Nervenzellen. Sie stießen dabei auf einen molekularen Mechanismus, der die Neuronenmigration im Neocortex steuert und damit die Entwicklung dieses besonderen Gehirnareals entscheidend beeinflusst. Eine Schlüsselrolle spielt dabei der Transkriptionsfaktor Bcl11a.
Das menschliche Gehirn ist ein biologisches Meisterwerk. Eines der Hochleistungszentren in dieser komplexen Architektur aus Milliarden von Nervenzellen ist die Großhirnrinde, auch Neocortex genannt. Aufgebaut ist diese Hirnregion, in der unter anderem das Sprachzentrum des Menschen verankert ist, aus sechs verschiedenen Schichten, die parallel zur Oberfläche des Gehirns verlaufen. Und in jeder dieser Schichten siedeln jeweils besondere Nervenzellen. Diese Neuronenpopulationen unterscheiden sich nicht nur in ihren Verschaltungsmustern, sondern sie besitzen sogar so etwas wie eine positionsabhängige Identität mit ganz spezifischen Eigenschaften.
Neue Erkenntnisse zur Entwicklung dieses besonderen Gehirnareals liefern nun Wissenschaftler um den Ulmer Mediziner Professor Stefan Britsch in der jüngsten Ausgabe der höchst renommierten Fachzeitschrift NEURON. „Eine Schlüsselrolle in diesem komplexen Prozess spielt die so genannte neuronale Migration. Denn die zellulären Wanderungsbewegungen sorgen dafür, dass die neuronalen Vorläuferzellen ihren jeweiligen Bestimmungsort in den unterschiedlichen Schichten des Neocortex finden, bevor sie dort ausreifen und sich in die schichtspezifischen neuronalen Schaltkreise integrieren“, erklärt Professor Stefan Britsch. Der Leiter des Instituts für Molekulare und Zelluläre Anatomie der Universität Ulm hat gemeinsam mit seinem Mitarbeiter Dr. Christoph Wiegreffe einen neuen molekularen Mechanismus entdeckt, über den die Entwicklung des Neocortex reguliert wird. In Zusammenarbeit mit Kooperationspartnern der Berliner Charité sowie Wissenschaftlern aus Großbritannien und den USA konnten die Ulmer Forscher zeigen, dass der Transkriptionsfaktor Bcl11a bei der Steuerung der neuronalen Migration im Neocortex eine entscheidende Rolle spielt.
Die Ulmer Forscher konnten außerdem nachweisen, dass über diesen Genschalter die Expression eines bestimmten „Wegfindungsproteins“ (Sema3c) aus der Gruppe der sogenannten Semaphorine beeinflusst wird, das die radiale Migration der Nervenzellen steuert. In dem zu Cell-Press gehörenden Fachjournal NEURON, das weltweit zu den führenden auf dem Gebiet der neurobiologischen Forschung zählt, konnten die Ulmer Forscher im Mausmodell zeigen, dass bei der vorderhirnspezifischen Mutation von Bcl11a nicht nur der Neocortex viel schmaler ist als im Normalfall, sondern auch die Schichtung des Gehirns nicht mehr klar abgegrenzt ist. „Wir konnten zudem Belege dafür liefern, dass fehlerhafte Wanderungsbewegungen von kortikalen Neuronen mit einer gestörten Polarität der Nervenzellen einhergehen“, ergänzt Dr. Christoph Wiegreffe.
Gleichwohl die Resultate das Ergebnis langwieriger Grundlagenforschung sind, haben sie zugleich erhebliche klinische Relevanz. So wurden vor kurzem erstmals Mutationen von Bcl11a im Menschen entdeckt, die mit einer gestörten Entwicklung des Großhirns einhergehen. Bei den Betroffenen verzögern sich dadurch Sprachentwicklung und intellektuelle Reifung. Auch sogenannte Autismus-Spektrum-Störungen sind auf subtile Fehler bei der Neuronenwanderung zurückzuführen. „Dabei spielen sowohl das Migrationsverhalten der neokortikalen Nervenzellen selbst eine Rolle als auch damit verbundene zelluläre `Identitätsprobleme´ und Verschaltungsstörungen“, so die Hirnforscher.
Bei ihren Forschungen gelangen den Wissenschaftlern übrigens faszinierende Einblicke in die neuronalen Migrationsprozesse. Per „Live Cell Imaging“, einer Methode zur Beobachtung von lebenden Zellen in ihrer natürlichen Umgebung, konnte das Forscherteam sogar die Wanderungsbewegungen einzelner Neuronen filmen. Neben klassischen konditionellen Gen-Knockout-Strategien in der Maus (loss-of-function-Ansatz) haben die Wissenschaftler zudem so genannte gain-of-function-Ansätze verwendet, um bestimmte Phänotypen der Mutation aufzuheben und damit die Funktion spezifischer Gene im Gehirn besser charakterisieren zu können. Das methodische Spektrum der Studie reichte daneben von molekularbiologischen und immunhistologischen Methoden bis hin zu Bildgebungsverfahren wie der konfokalen Mikroskopie und dem Live Cell Imaging.
Die Ulmer Wissenschaftler konnten damit nicht nur belegen, dass die mutationsbedingten Migrations- und Polaritätsdefekte zum Teil auf die Bcl11a vermittelte erhöhte Expression von Sema3c zurückzuführen sind, sondern es ist ihnen zudem gelungen, durch die Normalisierung des axonalen Wegfindungsproteins das Auftreten von Migrationsdefekten bei der Hirnentwicklung zu verhindern.
„Mit diesen neuen Erkenntnissen zur Neuronenwanderung konnten wir grundlegende Fragen bei der Gehirnentwicklung klären sowie ein besseres Verständnis für die Entstehung von Erkrankungen des Gehirns und des Nervensystems schaffen“, sind Britsch und Wiegreffe überzeugt. Gefördert wurde das Projekt von der Deutschen Forschungsgemeinschaft (DFG) und der Medizinischen Fakultät der Universität Ulm im Rahmen des so genannten Bausteinprogramms für junge Wissenschaftler.
Literatur: