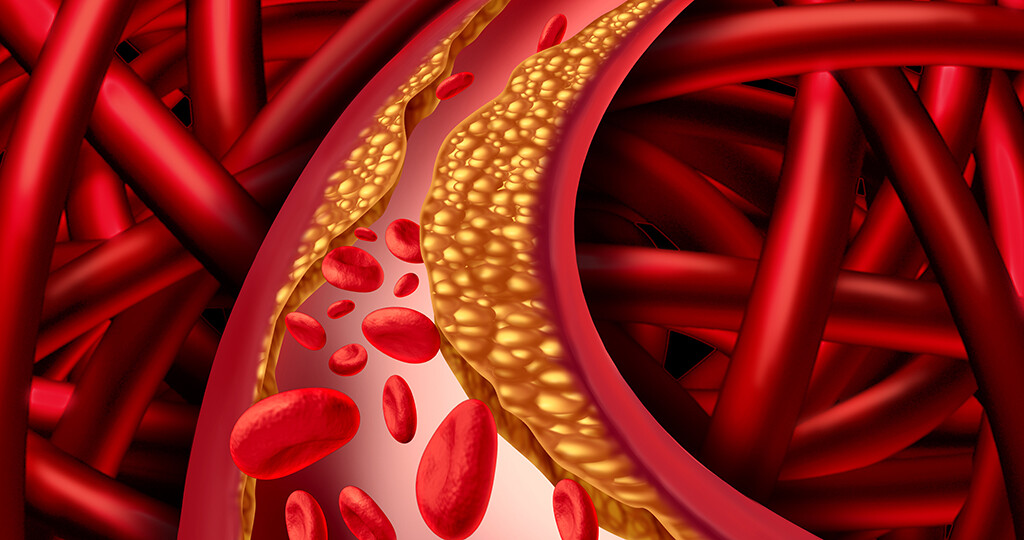
Bei Fettstoffwechselstörungen verändert sich die Zusammensetzung der Blutfette (Lipide), wobei meistens Cholesterin- und Triglyceridspiegel betroffen sind.
Die Europäische Gesellschaft für Kardiologie und die Europäische Gesellschaft für Atherosklerose empfehlen in ihren aktualisierten Leitlinien, dass der LDL-C-Wert besonders bei Patienten mit einem sehr hohen Risiko für Herz-Kreislauf-Erkrankungen soweit wie möglich gesenkt werden sollte. Gerade für Hochrisikogruppen ist im Zusammenhang mit Fettstoffwechselstörungen die dauerhafte Reduktion des LDL-Cholesterin-Wertes essentiell. Und zwar um das Risiko für Herz-Kreislauf-Erkrankungen zu reduzieren. Dazu zählen auch Patienten mit Familiärer Fettstoffwechselstörung (Hypercholesterinämie, FH), bei der es genetisch bedingt zu erhöhten Cholesterin-Werten kommt.
Bei Fettstoffwechselstörungen meist Cholesterin- und/oder Triglyceridspiegel betroffen
Fettstoffwechselstörungen sind Veränderungen der Zusammensetzung der qualitativen und/oder quantitativen sogenannten Blutfette (Lipide), wobei meistens der Cholesterin- und/oder der Triglyceridspiegel betroffen. Fettstoffwechselstörungen können viele exo- und endogene Ursachen und viele, oft sehr dramatische, Auswirkungen haben. Sie können auch als Folge verschiedener Erkrankungen, die den Stoffwechsel von Lipiden im Blutplasma betreffen, entstehen; weiters gibt es genetisch bedingte Fettstoffwechselstörungen, wie die verschiedenen Formen der sogenannten Familiären Hypercholesterinämie sowie erworbene, durch den Lebensstil bedingte (Ernährung, Bewegungsmangel) Fettstoffwechselstörungen. Wir beschäftigen uns heute vorwiegend mit den beiden letztgenannten.
Lipoproteine im Blut
Körpereigene Fette und durch die Nahrung zugeführte Fette werden, da sie nicht wasserlöslich sind, an Eiweißkörper gebunden im Blut transportiert, man spricht von Lipoproteinen. Vereinfacht gesagt: Befinden sich zu viele Lipoproteine im Blut, dringen diese vermehrt in die Gefäßwände ein und rufen eine Reihe chemischer Prozesse wie unter anderem Oxidation und eine Entzündungsreaktion hervor, die wesentlich zur Entstehung von Atherosklerose beiträgt.
Fettstoffwechselstörungen bzw. Lipidstoffwechselstörungen stellen also einen zentralen Faktor für die Entwicklung von Atherosklerose und in der Folge für die Entwicklung von koronarer Herzkrankheit, Herzinfarkt, Schlaganfall und anderer kardiovaskulärer Erkrankungen dar.
Atherosklerose ist eine Zivilisationserkrankung, die schon bei den alten Ägyptern und Griechen bekannt war. Dabei ist Atherosklerose nicht, wie früher fälschlich angenommen, durch eine kontinuierliche Zunahme der Dicke der Gefäßwand charakterisiert, sondern wird durch ein stufenweises, plötzliches Verengen des Gefäßvolumens verursacht, unter anderem durch Einlagerung von Blutfetten, Zellen und Kalk in Plaques, deren Ruptur (Riss des Gewebes) und teilweise oder komplett verschließende Thrombose (Blutgerinnsel).
Atherogenese – Wechselspiel zwischen Genen und Umwelt
Die Atherogenese, also die Entstehung von Atherosklerose basiert auf einem Wechselspiel von genetischen und Umweltfaktoren sowie dem Einfluss von Risikofaktoren, die für die verschiedenen Gefäßstrombahnen offenbar eine unterschiedliche Bedeutung aufweisen: So sind Blutfette und Zigarettenrauchen vor allem mit Veränderungen an den Herzkranzgefäßen; Zigarettenrauchen, erhöhtes Lipoprotein (a) und metabolisches Syndrom vorwiegend mit der peripheren arteriellen Verschlusskrankheit assoziiert.
Atherosklerotische Gefäßveränderungen können schon im Ungeborenen nachgewiesen werden, wenn zum Beispiel die Mutter raucht bzw. eine Fettstoffwechselstörung aufweist. Diese Veränderungen sind postpartal allerdings offensichtlich vollständig rückbildungsfähig. Liegt mehr als ein Risikofaktor vor, führt das meist zur überadditiven Erhöhung des Risikos.
Screening bei Familiärer Hypercholesterinämie
In der heterozygoten Form erfolgt die klinische Manifestation der Familiären Hypercholesterinämie meist um das 40. bis 50. Lebensjahr, in der homozygoten kann eine solche schon um das fünfte Lebensjahr beobachtet werden.
Familiäre Hypercholesterinämie ist eine autosomal dominante Erbkrankheit (bereits der Defekt eines Allels aus einem der beiden homologen Chromosomen genügt, um die Erkrankung auszulösen; das „Nachbar-Gen“ kann den Defekt nicht ausgleichen). Hat man diesen Gendefekt von nur einem Elternteil geerbt, spricht man von heterozygoter Familiärer Hypercholesterinämie, hat man ihn von beiden Elternteilen, liegt die homozygote Familiäre Hypercholesterinämie. In beiden Fällen kann man das LDL-Cholesterin nicht mehr ausreichend durch die Leberrezeptoren aus dem Blut filtern. Wobei der LDL-Spiegel, wenn man nicht behandelt, dramatisch ansteigt. Schon im Kindes- und Jugendalter kann es, je nach Form und Ausprägung, zum Auftreten von Herzinfarkten kommen.
Da mehr als 90% der frühen Ereignisse in weniger als 10% der Familien aggregiert sind, ist bei einem vorzeitigen Ereignis vor dem 55. Lebensjahr ein Screening sämtlicher Blutsverwandten („Rettet die Enkel“) absolut nötig und auch ökonomisch effizient und sinnvoll. Liegt keine frühe familiäre Manifestation vor, ist dennoch eine Cholesterinbestimmung erstmals zum Schuleintritt des Kindes empfohlen (Konsens) bzw. die einmalige Bestimmung des Lipoprotein(a), das sich im Laufe des Lebens nicht signifikant ändert, erforderlich (VUMA-Papier 1996). Zur Stellung der Stellung der Diagnose sollten die Blutfettwerte herangezogen werden.
Grenzwerte zu Cholesterin und Triglyceriden für die Therapieentscheidung bei Fettstoffwechselstörungen
In verschiedensten Ländern, vor allem den USA, wird zur Therapieentscheidung das Risikoprofil angegeben. Bei familiären Störungen wird somit das Risiko massiv unterschätzt, während bei den nichtfamiliären Formen das Risiko generell überschätzt wird. Diese Überschätzung ist vor allem bei Personen mit besonders schlechtem Lebensstil am höchsten. Nimmt man das VUMA-Papier von 1996, hat sich an den damals festgelegten Werten (siehe Tabelle 1) eigentlich nichts geändert, abgesehen davon, dass bei klinischer Manifestation der Atherosklerose und Progression ein LDL-Cholesterin von unter 70mg/dl angestrebt werden soll. Sämtliche anderen nationalen wie internationalen Empfehlungen wurden inzwischen wiederholt abgeändert, redigiert und modifiziert, häufig nachgeahmt, haben aber nichts Neues erbracht.
Einteilung der Fettstoffwechselstörungen
Wie teilt man die Fettstoffwechselstörungen nun ein, entweder nach der Typisierung nach Fredrickson, nach verschiedenen Typen (I – V) oder einfach nur nach Parametern wie Cholesterin, HDL und Lp(a)?
Teilt man nach der Veränderung der Lipide ein, ergibt sich folgendes Bild:
- Hypercholesterinämie (erhöhtes Cholesterin)
- Hypertriglyceridämie (erhöhte Triglyceride)
- Kombinierte Hyperlipidämie (erhöhtes Cholesterin und erhöhte Triglyceride)
Teilt man nach der Veränderung der Lipoproteine ein, ergibt sich folgendes Bild:
- Hypoalphalipoproteinämie (erniedrigtes HDL, high-density-lipoprotein)
- Hyperbetalipoproteinämie (erhöhtes „schlechtes“ LDL und reduziertes „gutes“ HDL)
- Erhöhtes Lipoprotein(a) bzw. Kombinationen
Beck et al., Cholesterin 2. ACCC 2002
Welcher Parameter ist der wertvollste? LDL-Cholesterin ist ein wesentlicher Parameter, HDL-Cholesterin ist aber bei metabolischem Syndrom aussagekräftiger. Liegt ein erhöhtes Lipoprotein(a) vor, ist das non-HDL LP der aussagekräftigste Parameter. Was also ist nun wichtig und richtig?
In der westlichen Welt sind die sogenannten Hyperlipidämien von großer klinischer Bedeutung. Und zwar stehen dabei die Erhöhung von Cholesterin und Triglyceriden mit oftmals niedrigem HDL im Vordergrund. Schon Rudolf Virchow, der Begründer der Zellpathologie, schrieb der chronischen Entzündung eine wesentliche Bedeutung in der Atherogenese zu. Zigarettenrauchen, Parodontitis und Übergewicht (vor allem Bauchfett) führen zu einer chronischen Entzündung. Die Kombination der Störung des Fettstoffwechsels (erhöhtes LDL und reduziertes HDL), des Glucosestoffwechsels (Insulinresistenz), vergemeinschaftet mit Übergewicht (abdominelle Adipositas, „Bauchfettsucht“) und Hypertonie (Bluthochdruck) wird unter dem Begriff Metabolisches Syndrom, „Deadly Quartett“ (nach Reaven) oder “Fettkrankheit“ (nach Kritz) subsumiert.
Fazit
Die Rückbildung der Atherosklerose ist möglich, dauert aber im Regelfall mindestens fünfmal so lange wie deren Entstehung. Erstaunlicherweise scheint aber die Stabilisierung der atherosklerotischen Läsion (der Gefäßoberfläche bzw. des Endothels) der entscheidende Faktor zu sein, der bereits nach wenigen Tagen oder Wochen mit einer massiv senkenden Lipidtherapie (zum Teil auch durch Non-Lipid-Effekte) erreicht werden kann.
Quelle:
2019 Guidelines on Dyslipidaemias (Management of) – ESC Clinical Guidelines Practice.