Streik der zellulären Müllabfuhr
Ein internationales Team unter Leitung von Grundlagenforschern der Universitätsmedizin Göttingen entdeckt: Zellen können ihre Müllabfuhr regulieren und sogar selbst einen Streik auslösen. Ein Regulator namens miR-101 verhindert die richtige Zusammensetzung des Proteasoms. Publiziert in der renommierten Fachzeitschrift „Molecular Cell“, Nr. 119, 6. Juli 2015.
Auf eine funktionierende Müllabfuhr sind auch einzelne Zellen angewiesen. Ihre Recycling-Tonne ist das „Proteasom“ und gleicht in seiner Form tatsächlich einer Tonne. Im Proteasom werden überschüssige Eiweißmoleküle der Zelle zerhackt, die Bausteine können neu verwendet werden. Bisherige Kenntnisse über die Mechanismen der zellulären Müllabfuhr werden bereits in der Krebstherapie genutzt, um Tumorzellen gezielt „zuzumüllen“. Dabei setzt man bislang auf „Sabotage“ und die Hilfe pharmakologischer Wirkstoffe, um das Proteasom in seiner Arbeit hemmen.

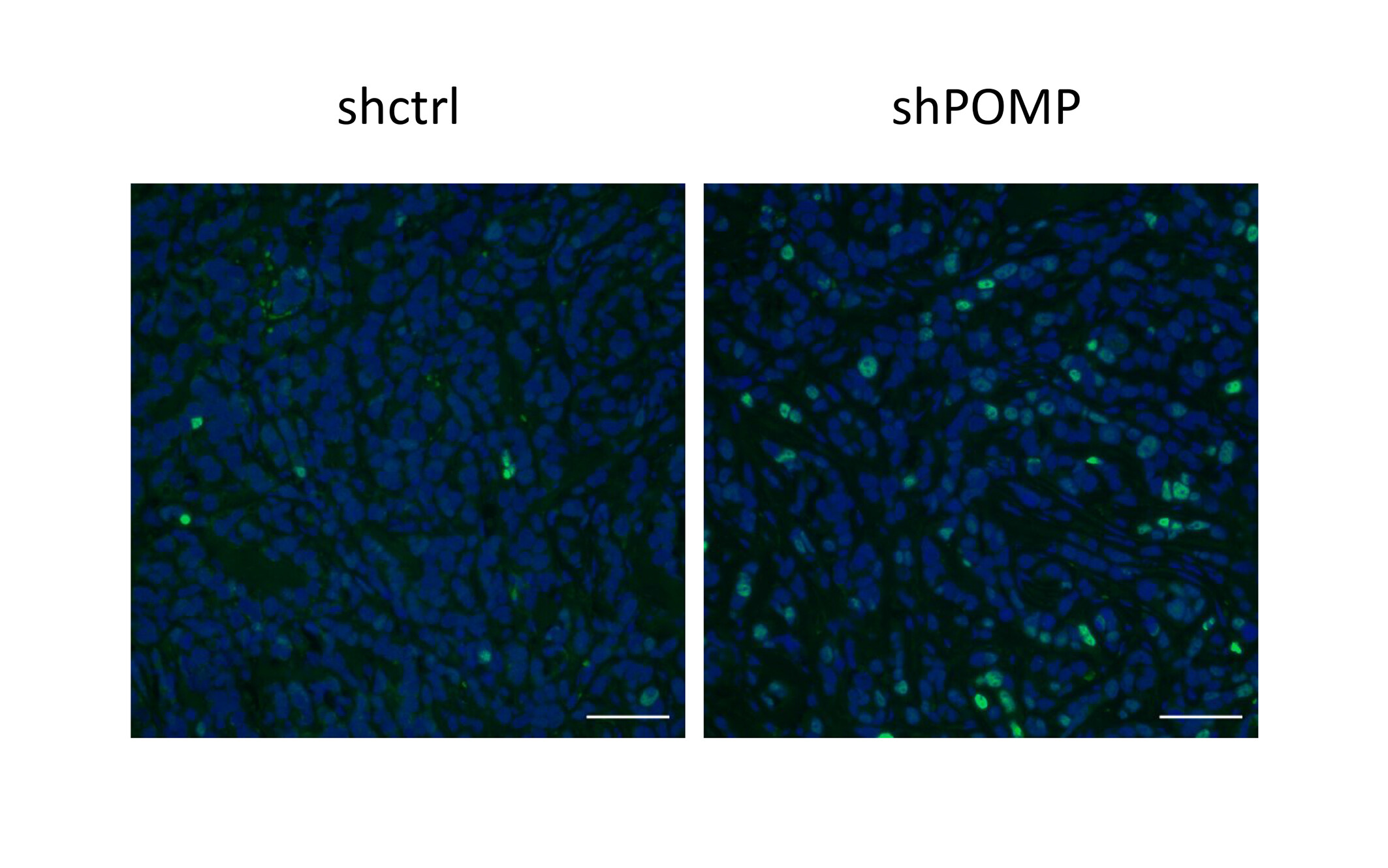
Streikaufruf durch Hemmung der Proteasom-Reifung. Abb. links zeigt einen unbehandelter Tumor; Abb. rechts zeigt einen Tumor, bei dem der Proteasom-Reifungsfaktor POMP entfernt wurde. Dies führt zur Anhäufung des Tumorsuppressors p53, hier durch eine Immunfluoreszenzfärbung (grün) nachgewiesen.
Dass die Zelle sogar selbst über einen natürlichen Regulator der Proteasom-Funktion verfügt, hat nun ein internationales Forscherteam um Dr. Xin Zhang und Prof. Dr. Matthias Dobbelstein, beide Institut für Molekulare Onkologie der Universitätsmedizin Göttingen (UMG), entdeckt. Die Wissenschaftler identifizierten ein zelluläres Molekül, das einen regelrechten Streik der proteasomalen Müllabfuhr auslöst. Finanziert wurde das Projekt durch die Deutsche Krebshilfe (DKH). Die Ergebnisse wurden am 2. Juli 2015 in der renommierten Zeitschrift „Molecular Cell“ online veröffentlicht.

Der „Gewerkschaftsboss“ in dem zellulären Streikgeschehen ist die Ribonukleinsäure „microRNA 101“ oder kurz „miR-101“. miR-101 hemmt die Herstellung eines Eiweißmoleküls mit dem Namen „proteasome maturation protein“, kurz POMP. Trotz des pompösen Namens ist POMP nur ein Helfer beim Zusammenbau der proteasomalen Recycling-Tonne. Ohne POMP werden die Proteasomen allerdings nicht mehr korrekt zusammengesetzt. Die zelluläre Recycling-Maschinerie steht still.
Wozu benötigt die Zelle eine solche Streik-Option?
„Möglicherweise steckt ein Mechanismus dahinter, der die Entstehung von Krebs ver-hindern soll“, sagt Prof. Dobbelstein. Indizien für eine solche Annahme fanden die Forscher ebenfalls: Tumoren wachsen umso schneller, je weniger miR-101 und je mehr POMP sie haben. Diese Ergebnisse entstanden in Zusammenarbeit mit der Klinik für Allgemein-,Viszeral- und Kinderchirurgie (Direktor: Prof. Dr. Michael Ghadimi) und der Arbeitsgruppe um Prof. Dr. Tim Beissbarth am Institut für Medizinische Statistik (Direktor: Prof. Dr. Tim Friede) der UMG.
Künstlich hergestellte Proteasom-Inhibitoren gibt es schon seit Jahren. Die nun vorgelegten Ergebnisse zeigen, dass die Natur längst etwas Ähnliches verwendet. Mir-101 kann das zelluläre Recycling anpassen und stellt möglicherweise eine Art Notbremse dar, um Krebs zu verhindern.
Eine klinische Anwendung der Ergebnisse ist derzeit noch nicht in Sicht. Die Göttinger Forscher sind aber zuversichtlich, dass die Arbeit helfen kann, neue Strategien zur Proteasom-Inhibition zu entwerfen. „Die Anhäufung von Eiweiß-Müll oder proteotoxischer Stress ist ein häufiges Phänomen in Krebszellen“, sagt Dobbelstein. „Diese Stressform sollten wir gezielt verstärken, um Tumorwachstum zu verhindern“.