Pulmonale Hypertonie lässt sich heute effektiver behandeln, Klassifikation und Pathophysiologie spielen für Diagnose und Therapie eine wichtige Rolle.
Pulmonale Hypertonie (PH) zeigt komplexe Mechanismen der Pathophysiologie, die vor allem durch die Klassifikation der Erkrankung erkennbar sind. Diese Mechanismen stellen einen wichtigen Ansatzpunkt für eine effektive Behandlung dar.
Die pulmonale Hypertonie wird nach dem Schweregrad und dem Ansprechen auf kurz wirksame Vasodilatantien medikamentös behandelt. Regelmäßige Evaluationen und eventuelle Therapieumstellungen oder -kombinationen sind ebenfalls wichtig.
Trotz aller Fortschritte der medikamentösen Therapie stellen die atriale Septostomie und Lungentransplantation immer noch wichtige therapeutische Optionen dar.
Pulmonale Hypertonie: Klassifikation
Während man im vorigen Jahrhundert pulmonale Hypertonie (PH) einfach zwischen primäre und sekundäre unterschieden hatte, wurden beim zweiten Weltkonferenz zu Pulmonale Hypertonie in Evian, 1998, insgesamt 5 Klassen für pulmonale Hypertonie definiert. Inklusive der so genannten pulmonal arteriellen Hypertonie (PAH). Bei der dritten Weltkonferenz in Venedig, 2003, wurde die Klassifikation nochmals modifiziert. Man unterschied damals
- die pulmonal arterielle Hypertonie (PAH) von 4 anderen Gruppen, bei denen die PH eine Folgeerscheinung einer chronischen Erkrankung ist. Diese sind
- Linksherzerkrankungen,
- Lungenkrankheiten bzw. Hypoxie,
- die chronisch thromboembolische PH und
- sonstige definierte seltene Krankheiten mit direktem Befall der Lungengefäße, wie etwa die Sarkoidose oder Histiozytosis X.
Die PAH-Gruppe enthiellt die idiopathische Form (IPAH), früher PPH, die familiäre Form (FPAH), früher ebenfalls PPH, so genannte assoziierte Formen (APAH), die pulmonal veno-okklusive Erkrankung und die persistiernde PH der Neugeborenen.
Zu den APAH gehören Kollagenosen, angeborene links-rechts Shuntvitien, die portale Hypertension, HIV-Infektion, Appetitzügler and andere Drogen, Splenektomie, Hämoglobinopathien, myelodysplastische Syndrome. Das bedeutet, dass eine pulmonal arterielle Hypertonie letztlich dadurch definiert ist, dass die genannten anderen Krankheiten (Gruppe 2–5) als Ursache ausgeschlossen sind.
Pulmonale Hypertonie: Pathophysiologie
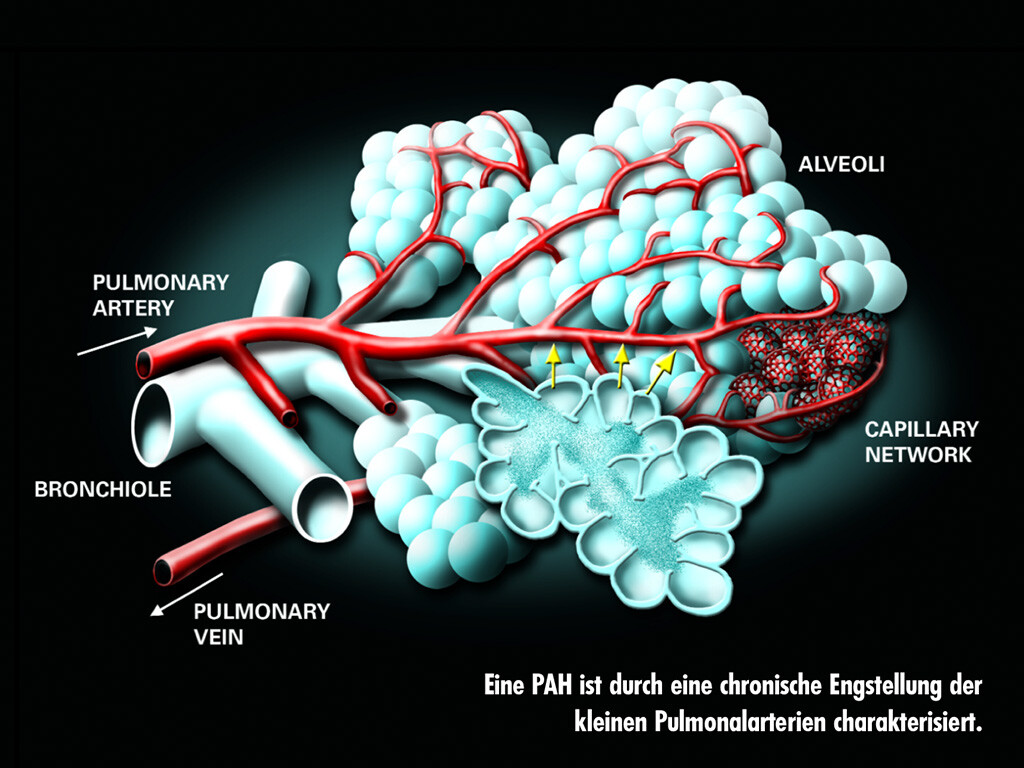
Eine PAH ist durch eine chronische Engstellung der kleinen Pulmonalarterien charakterisiert. Im histologischen Präparat erkennt man ein deutlich verkleinertes Lumen, bedingt durch eine Intimaverdickung und -fibrose in Kombination mit einer mehr oder weniger stark ausgeprägten Mediahypertrophie und einer Hypertrophie der Adventitia.
Keine Gefäßwandschicht wird also von den proliferativen Veränderungen ausgelassen. Offenbar besteht ein Ungleichgewicht zwischen Apoptose und Proliferation der beteiligten Zellen.
Es ist letztlich nicht bekannt, bei welchem Zelltyp in den kleinen Pulmonalarterien die Krankheit wirklich beginnt. Umso weniger ist bekannt, welcher pathologische Mechanismus als primär anzusehen ist. Von den familiären Formen (FPAH) wissen wir, dass Defekte im bone morphogenetic protein receptor 2 (BMPR-2) und im ALK1 Rezeptor mit 20% Wahrscheinlichkeit zu einer PAH führen.
Hier ist die primäre Ursache bekannt, allerdings ist der Mechanismus, über den die pulmonale Hypertonie bei dieser Mutation entsteht, noch nicht bekannt. Interessant ist, dass ALK1 Mutationen bei den meisten Patienten zur hereditären Teleangiektasie (M. Osler) führen, und nur in der Minderzahl zu pulmonale Hypertonie. Es müssen also weitere genetische Faktoren vermutet werden, die den Phänotyp letztlich bestimmen.
Interessant ist weiterhin, dass auch Patienten ohne Keimlinienmutation eine verminderte BMPR1 Expression in der Lunge aufweisen. Man muss daher davon ausgehen, dass pulmonale Hypertonie einen Effekt bewirkt, der dazu führt, dass sich die Krankheit perpetuiert (Teufelskreis).
Weitere Teufelskreise betreffen die verminderte Prostacyclin-Synthase und NO Synthase sowie die Kaliumkanalexpression und die vermehrt exprimierte Endothelin Synthase. Ein mechanischer Teufelskreis ergibt sich durch Druckschäden an den Gefäßen, welche von der PH induziert werden und sekundär zum Gefäßwachstum führen. Insgesamt ist von einem multikausalen Geschehen auszugehen, dessen Details noch nicht genau bekannt sind.
Nizza-Klassifikation teilt die pulmonale Hypertonie in fünf Klassen und mehrere Subklassen ein
Die fünf Klassen der Nizza-Klassifikation berücksichtigen die jeweilige Ursache der pulmonalen Hypertonie. Die Nizza-Klassifikation wurde im Jahre 2013 auf der 5. Weltkonferenz festgelegt und löste damals die Dana-Point-Klassifikation aus dem Jahr 2008 ab.
- Pulmonalarterielle Hypertonie – pulmonale venookklusive Erkrankung (PVOD) – pulmonalkapilläre Hämangiomatose (PCH) – persistierende pulmonalarterielle Hypertonie des Neugeborenen (PPHN)
- PH bei Erkrankungen des linken Herzens
- Pulmonale Hypertonie bei Lungenerkrankung und/oder Hypoxie
- PH aufgrund chronischer Thrombembolien (CTEPH)
- Pulmonale Hypertonie mit unklaren multifaktoriellen Mechanismen
Nizza-Subklassen
1 Pulmonal Arterielle Hypertonie (PAH)
1.1 Idiopathische pulmonalarterielle Hypertonie (IPAH)
1.2 Hereditäre pulmonalarterielle Hypertonie (HPAH) – BMPR2, ALK1, Endoglin (mit oder ohne hereditärer hämorrhagischer Teleangiektasie), Unbekannt
1.3 Arzneimittel- und toxininduziert
1.4 Assoziierte Pulmonalarterielle Hypertonie (APAH); – Kollagenosen, HIV-Infektion, portaler Hypertonie, angeborenen systemisch-pulmonalen Shunts (u. a. Herzfehler), Bilharziose
2 Pulmonale Hypertonie bei Linksherzerkrankungen
2.1 Systolische Dysfunktion
2.2 Diastolische Dysfunktion
2.3 Herzklappenerkrankungen (Mitral- oder Aortenklappenfehler)
3 Pulmonale Hypertonie assoziiert mit Lungenerkrankungen und/oder Hypoxie
3.1 Chronisch obstruktive Lungenkrankheit
3.2 Interstitielle Lungenkrankheit
3.3 Schlafapnoesyndrom
3.4 Erkrankungen mit alveolärer Hypoventilation
3.5 Chronische Höhenerkrankung
3.6 Pulmonale Entwicklungsstörungen, anlagebedingte Fehlbildung
4 Pulmonale Hypertonie aufgrund chronischer thrombotischer und/oder embolischer Erkrankungen (CTEPH) – Thromboembolie der proximalen Lungenarterien, Obstruktion der distalen Lungenarterien, Lungenembolie (Tumor, Parasiten, Fremdkörper)
5 Sonstige mit unklaren multifaktoriellen Mechanismen
5.1 Hämatologische Erkrankungen: Chronisch hämolytische Anämie, Myeloproliferative Erkrankungen, Zustand nach einer Splenektomie
5.2 Systemische Erkrankungen: Sarkoidose, pulmonale Langerhanszellenhistiozytose, Lymphangioleiomyomatose, Neurofibromatose, Vaskulitis
5.3 Metabolische Erkrankungen: Glykogenspeicherkrankheit, Morbus Gaucher, Schilddrüsenerkrankungen
5.4 Andere: Obstruktion durch Tumore, fibrosierende Mediastinitis, chronischer Nierenausfall mit Dialyse
Literatur:
Lauren Krowl; Pratibha Kaul. Pulmonary Idiopathic Hypertension. StatPearls [Internet]. Last Update: May 30, 2020.
Hoeper MM, Ghofrani HA, Grünig E, Klose H, Olschewski H, Rosenkranz S. Pulmonary Hypertension. Dtsch Arztebl Int. 2017;114(5):73-84. doi:10.3238/arztebl.2017.0073
Hansmann G. Pulmonary Hypertension in Infants, Children, and Young Adults. J Am Coll Cardiol. 2017 May 23;69(20):2551-2569. doi: 10.1016/j.jacc.2017.03.575. PMID: 28521893.