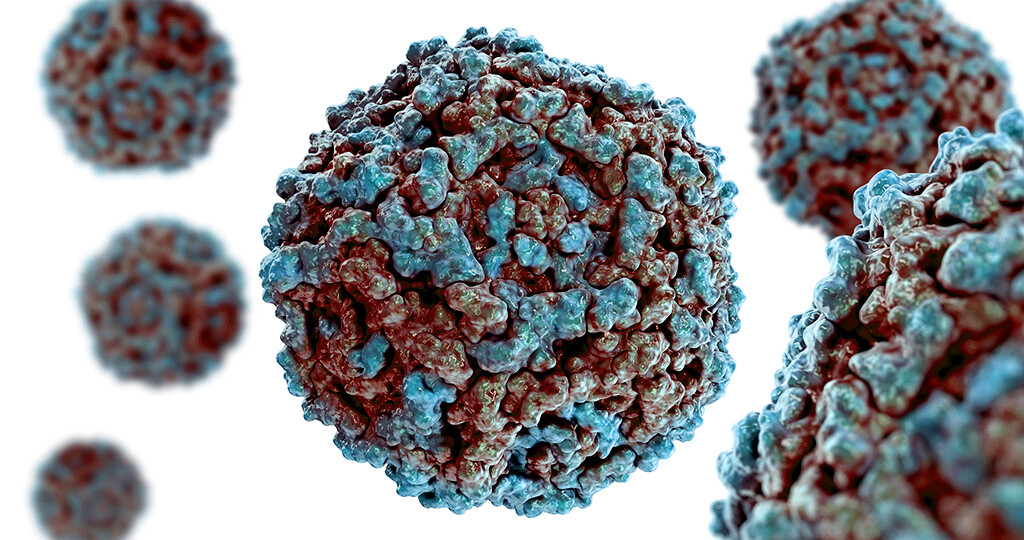
Eine Parvovirus B19-Infektion könnte an der Entstehung von Autoimmunerkrankungen wie Rheuma beteiligt sein, das Parvovirus B19 muss aber nicht zwingend Auslöser sein.
Ein Teilgebiet der virologischen Forschung beschäftigt sich mit der Frage, welche Rolle Virusinfektionen bei der Entstehung von Autoimmunkrankheiten spielen. Ein Virus, dem immer wieder eine kausale Rolle bei der Entstehung von Autoimmunerkrankungen wie Rheuma zugeschrieben wird, ist das Parvovirus B19 (B19V). Wobei man eine Parvovirus B19-Infektion eigentlich vor allem mit Ringelröteln und Komplikationen in der Schwangerschaft in Verbindung bringt.
Parvovirus B19 (B19V)
Parvovirus B19 ist ein kleines, einzelsträngiges DNA Virus, das über Tröpfchen übertragen wird. Primärinfektionen mit dem Parvovirus B19 erfolgen meist im Kindesalter und bei jungen Erwachsenen. Wobei ein Großteil der Infektionen asymptomatisch bleibt.
Wenn Symptome auftreten, dann entwickelt sich bei Infizierten nach einer Inkubationszeit von etwa 14 Tagen typischerweise das klinische Bild der Ringelröteln (makulo-papulöses Exanthem und Fieber). Vor allem im Erwachsenenalter kann das B19V Autoimmunerkrankungen wie Arthritiden mit Gelenkschmerzen auslösen.
Das Parvovirus B19 besitzt einen ausgeprägten Tropismus für Erythroblasten (Vorläuferzellen der roten Blutzellen). Als Tropismus bezeichnet man in der Virologie die Fähigkeit eines Virus, eine bestimmte Sorte von Zellen oder bestimmte Gewebe zu infizieren. Wobei sie sich dort dann weiter vermehren.
Das bewirkt jedenfalls, dass transiente Retikulozytopenien und Anämien zu weiteren möglichen klinischen Manifestationsformen der akuten B19V-Infektion gehören.
Bei Immunsupprimierten und Personen mit Blutbildungsstörungen können diese mitunter schwere aplastische Krisen auslösen.
Komplikationen
Der Tropismus des Parvovirus B19 für Erythroblasten ist außerdem für mögliche Komplikationen in der Schwangerschaft verantwortlich, bei denen es nach intrauteriner B19V-Transmission zu fetalen Anämien und dadurch zum Hydrops fetalis kommen kann.
Weitere schwere Komplikationen, die mit einer Parvovirus B19-Infektion in Zusammenhang stehen, sind Myokarditiden, Hepatitiden, Thrombo- und Leukozytopenien sowie neurologische Symptome, die aber gottseidank selten auftreten.
Im Rahmen der akuten Parvovirus B19-Infektion kommt es in der Regel zu einer starken Immunantwort des humoralen und zellulären Immunsystems, wobei das Ausmaß der Immunantwort Einfluss darauf hat, ob und wie stark sich bei Infizierten Ausschlag und Arthritis ausbilden.
Pathogenetisch spielen dabei die Bildung und die Ablagerung von Immunkomplexen im Gewebe eine wichtige Rolle, aber auch der genetische Hintergrund und das Ausmaß der Produktion von entzündungssteigernden Zytokinen (Interferon-alpha, Tumor Nekrose Faktor-alpha) scheint mit dem Ausmaß der Symptomatik zu korrelieren (so zeigen Menschen mit bestimmten HLA-Typen wie z.B. HLA-B49 stärkere Zytokinantworten und häufiger Symptome).
Die bedeutende Rolle des Immunsystems bei der Pathogenese der Parvovirus B19-Infektion legt die Frage nahe, ob das Parvovirus B19 überschießende Immunantworten und damit die Entstehung von Autoimmunkrankheiten begünstigen könnte.
Parvovirus B19 und Rheuma
Dafür spricht, dass was bei der klinischen Betreuung von Patienten mit Autoimmunkrankheiten immer wieder beobachtet wurde. Und zwar, dass Parvovirus B19-Infektionen, die ohnehin klinisch ähnliche Symptome (Fieber, Ausschlag, Gelenkbeschwerden) wie bestimmte Erkrankungen dieses Rheuma-Formenkreises (systemischer Lupus erythematodes, rheumatoide Arthritis oder juvenile idiopathische Arthritis) verursachen, deren Schübe auslösen beziehungsweise deren klinische Ausprägung verstärken konnten.
Im Lauf der letzten Jahre wurden diesbezüglich einige Fallberichte publiziert, bei denen es im direkten Anschluss einer B19V-Infektion zum Ausbruch einer rheumatoiden oder juvenilen idiopathischen Arthritis kam. Inzwischen liegen außerdem Einzelbeobachtungen vor, die B19V mit der Entstehung von verschiedenen Autoimmunkrankheiten wie z.B. Myositiden, Vaskulitiden, Typ 1 Diabetes, Hashimoto Thyreoiditis und Glomerulonephritis in Verbindung bringen.
Bildung von Autoimmunantikörpern
Die funktionelle Grundlage für den Zusammenhang zwischen dem Parvovirus B19 und Autoimmunerkrankungen könnte die Tatsache darstellen, dass es bei einem Teil der mit dem Parvovirus B19 Infizierten zur Bildung von Autoimmunantikörpern kommt.
Bereits im Jahr 1989 beobachteten japanische Forscher, dass es dabei zur Bildung von bestimmten Autoantikörpern (Antinukleäre Antikörper und Rheumafaktor) kommt. Und zwar solche, die man auch beim systemischen Lupus Erythematodes oder bei rheumatoider Arthritis finden kann. (Sasaki T et al., J Rheumatol 1989, 16: 708–709.)
Bei einem Teil der mit Parvovirus B19 infizierten Personen wurde sogar ein sehr breites Spektrum von Autoantikörpern (z.B. Antikörper gegen citrullinierte Peptide und Kardiolipin) gefunden, die gegen eine Vielzahl unterschiedlicher Gewebstypen gerichtet sind.
Molekulare Mimikry
Die B19V-Infektion verursacht aber nicht nur durch polyspezifische Stimulation die Bildung von Autoantikörpern. Sowohl in Tierversuchen mit Mäusen, die mit bestimmten viralen Proteinen immunisiert wurden, als auch durch Aufreinigung von Seren von B19V infizierten Personen, konnte gezeigt werden, dass auch jene Antikörper, die spezifisch gegen das Parvovirus B19 gerichtet sind, Selbstantigene körpereigener Strukturen (Kollagen II, Keratin, Kardiolipin u.a.) binden (Lunardi C et al., Eur J Immunol 1998, 28:936–48).
Die Ursache dieses Phänomens ist wahrscheinlich „molekulare Mimikry“. Damit bezeichnet man einen evolutionär erworbenen Evasionsmechanismus. Wobei dieser es dem Virus ermöglicht, durch Ähnlichkeit seiner Bestandteile mit körpereigenen Strukturen der Erkennung durch das Immunsystems zu entgehen.
Ein besonders interessantes Ergebnis der genannten Studien war, dass der Nachweis der autoimmun wirksamen Antikörper mit der klinischen Symptomatik korrelierte. Antikörper aus Seren von Patienten mit Ausschlag reagierten mit Keratin, Antikörper aus Seren von Patienten mit Gelenkschmerzen mit Kollagen II. Womöglich beeinflussen die gebildeten Autoantikörper also auch, ob sich eine klinische Symptomatik ausbildet.
Fazit
Man kann also nachweisen, dass es bei einem Teil der B19V-Infektionen zur Bildung von Autoantikörper kommt. Damit kann man schließlich auch zusammenfassend sagen, dass die Möglichkeit, dass das Parvovirus B19 an der Entstehung von Autoimmunerkrankungen beispielsweise bei Rheuma beteiligt ist, im Grunde genommen besteht.
Es muss jedoch betont werden, dass die Rolle von Parvovirus B19 als (alleiniger) Auslöser dieser Autoimmunerkrankungen keineswegs gesichert ist. So liegen auch Beobachtungen vor, dass Patienten mit Autoimmunkrankheiten im Vergleich zu Gesunden keine gehäufte B19V-Durchseuchung aufweisen. Das unterstreicht wiederum die multifaktorielle Genese dieser Erkrankungen.
Teilweise ist es jedenfalls sehr schwer, die bisherigen Studien bei der ständig fortschreitenden Forschung richtig zu interpretieren. Beispielsweise liegen etliche Studien vor, bei denen Wissenschaftler eine Parvovirus B19-DNA bei Patienten mit Autoimmunerkrankungen in den Herden der entzündenden Rheuma-Gelenke nachweisen konnten.
Inzwischen gilt es aber als gesichert, dass das Parvovirus B19 bei einem Großteil der Infizierten in verschiedenen Geweben persistiert. Das erschwert es, die kausale Rolle des Parvovirus B19 bei der Entstehung von Autoimmunerkrankungen abschließend zu bewerten.
Nichtsdestotrotz ist diese hochinteressante Frage Inhalt aktueller Forschungsarbeit, über deren Fortschritt wir an dieser Stelle weiter berichten werden.
Quelle:
VIRUSEPIDEMIOLOGISCHE INFORMATION” NR. 23/16-8. Ass.Prof.Priv.Doz.Dr.med. Lukas Weseslindtner.