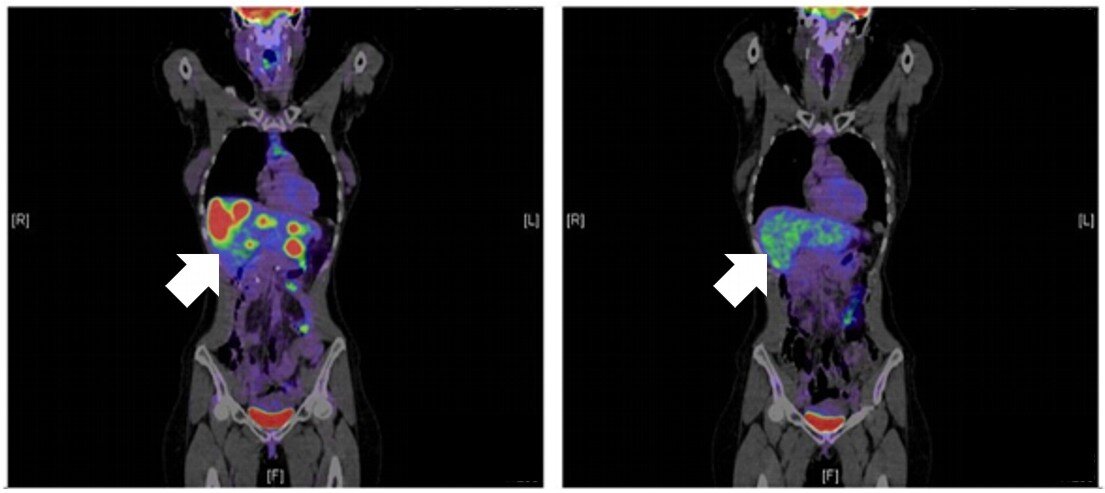
Eine neue Immuntherapie bei Darmkrebs mit Metastasen beeinflusst das Immunsystem, damit es mittels Makrophagen die Krebszellen bekämpft und zerstört.
Darmkrebs mit Metastasen ist schwer zu behandeln. Wissenschaftler des Nationalen Centrums für Tumorerkrankungen (NCT) und des Universitätsklinikums Heidelberg in Zusammenarbeit mit dem Deutschen Krebsforschungszentrum (DKFZ) haben jetzt herausgefunden, dass sich die Metastasen das Immunsystem zum Komplizen machen. Dabei spielen die Makrophagen, auch Fresszellen genannt, eine zentrale Rolle.
Offenbar werden sie in der Leber von den Metastasen derart beeinflusst, dass sie Tumorzellen helfen zu wachsen und sich zu verbreiten. Ursache ist ein Signalweg, den auch das HI-Virus als Eintrittspforte in menschliche Zellen nutzt. Ein Hemmstoff wird bereits bei HIV-Infizierten therapeutisch eingesetzt. Die Wissenschaftler und Ärzte haben die Wirkung des Medikaments nun in präklinischen Laborversuchen und in einer anschließenden Studie an 14 Patienten mit metastasiertem Darmkrebs erfolgreich getestet. Die Ergebnisse wurden jetzt in der Fachzeitschrift Cancer Cell publiziert.
Aktuell geringe Therapieoptionen bei fortgeschrittenem, nicht-operablem Darmkrebs mit Metastasen
Die Lebenserwartung von Patienten mit nicht-operablem Darmkrebs mit Metastasen beträgt etwa 24 Monate. In dem fortgeschrittenen Stadium sind die noch verfügbaren Therapieoptionen gering. Immuntherapeutische Ansätze sind bisher wenig erfolgreich, obwohl sich Immunzellen und deren Signalstoffe in der Nähe der Krebszellen nachweisen lassen.
Aktuelle Immuntherapien haben das Ziel, die erworbene Immunabwehr zu stärken. Dabei sollen vor allem die T-Zellen gegen die Tumorzellen aktiviert werden. Den Wissenschaftlern aus Heidelberg und Hannover ist es nun gelungen, auch den angeborenen Teil des Immunsystems zu mobilisieren. Dazu haben sie in Laborversuchen die Immunzellen, insbesondere die Makrophagen, aus dem Gewebe um Lebermetastasen von Darmkrebspatienten genauer untersucht.
„Ursprünglich vermutete man, dass auch die Immunabwehr in den Metastasen noch eine gewisse Wirksamkeit gegen den Tumor hat“, erklärt Dr. Niels Halama, Arzt und Wissenschaftler in der Abteilung Medizinische Onkologie am NCT. „Bei Darmkrebspatienten konnten wir jetzt zeigen, dass die Metastasen die Makrophagen in ihrer Umgebung so manipulieren, dass sie das Krebswachstum sogar fördern, statt es zu bekämpfen.“
Von tumorfördernd zu tumorbekämpfend
Eine wichtige Rolle spielt dabei das Signalprotein CCL5, das in der Regel an Entzündungsprozessen beteiligt ist, weil es Immunzellen in das Gewebe hineinzieht. Hohe Konzentrationen von CCL5 werden beispielsweise bei Krankheiten wie der rheumatoiden Arthritis, Multipler Sklerose und Morbus Hodgkin gefunden. Auch bei Brustkrebs-Metastasen wurden hohe Werte von CCL5 und damit verbunden ein tumorförderndes Milieu beobachtet.
Die Forscher fanden heraus, dass die T-Zellen in Nähe der Lebermetastase, CCL5 produzieren. Damit das Protein wirken kann, muss es an sein Gegenstück den Rezeptor CCR5 binden. Dieses Eiweiß befindet sich auch auf der Zelloberfläche von Makrophagen. Der Rezeptor CCR5 ist bereits aus der HIV-Forschung gut bekannt, denn das HI-Virus bindet an CCR5 und dringt so in die Zellen ein.
HIV-Medikament Maraviroc bei Patienten mit Darmkrebs und Metastasen eingesetzt
Ein bereits zugelassenes Medikament blockiert das Oberflächeneiweiß CCR5 und wird bei HIV-Infizierten therapeutisch genutzt. Die Wissenschaftler untersuchten die Wirksamkeit dieses HIV-Medikaments zunächst in präklinischen Versuchen an den Lebermetastasen. Die Blockade von CCR5 verwandelte die Makrophagen im Gewebe um die Metastase von tumorfördernd zu tumorbekämpfend.
Die „umprogrammierten“ Fresszellen konnten die Krebszellen zerstören und schonten gleichzeitig das umliegende gesunde Lebergewebe. „Die Untersuchungen haben unser Verständnis der Immunregulation bei Krebs verbessert. Es scheint, dass die CCL5-CCR5 Achse eine wichtige Bedeutung für die Aktivierung der Makrophagen hat. Und das nicht nur bei einer Virusinfektion wie bei HIV, sondern auch bei Krebserkrankungen“, erläutert die Immunologin Prof. Christine Falk von der Medizinischen Hochschule Hannover.
Nach den präklinischen Experimenten konnten die Forscher den Mechanismus in einer Phase-I-Studie mit 14 Patienten bestätigen und einen Rückgang einzelner Metastasen beobachten. „Die Daten der klinischen Studie zeigen eine sehr gute Verträglichkeit des HIV-Medikaments. Aber auch das Ansprechen in Kombination mit einer Chemotherapie ist vielversprechend“, berichtet Prof. Dirk Jäger, Ärztlicher Direktor am NCT und Sprecher des Forschungsschwerpunkts Tumorimmunologie am DKFZ. „Gerade für Darmkrebspatienten könnten neue Immuntherapien die Behandlungsmöglichkeiten massiv verbessern“, fügt Prof. Markus W. Büchler hinzu, Geschäftsführender Direktor der chirurgischen Universitätsklinik in Heidelberg.
Mit dieser Forschungsarbeit ist es zum ersten Mal gelungen, Makrophagen durch CCR5-Blockade gegen den Tumor zu reaktivieren. Die Wissenschaftler hoffen nun diese neue Immuntherapie, die das angeborene Immunsystem nutzt, weiter zu entwickeln. „Wir beginnen in Kürze weiterführende klinische Studien, um das Potential dieser neuen Therapieoption bei anderen Tumorerkrankungen besser zu verstehen“, ergänzt Niels Halama, der auch der Leiter der klinischen Studie bei metastasiertem Darmkrebs ist.
Quelle: Halama N, Zoernig I, Berthel A , Kahlert C, Klupp F, Suarez-Carmona M, Suetterlin T, Brand K, Krauss J, Lasitschka F, Lerchl T, Luckner-Minden C, Ulrich A, Koch M, Weitz J, Schneider M, Buechler M W, Zitvogel L, Herrmann T, Benner A, Kunz C, Luecke S, Springfeld C, Grabe N, Falk CS, Jaeger D (2016) Tumoral immune cell exploitation in colorectal cancer liver metastases can be targeted effectively by anti-CCR5 therapy in cancer patients. Cancer Cell 29: 587-601