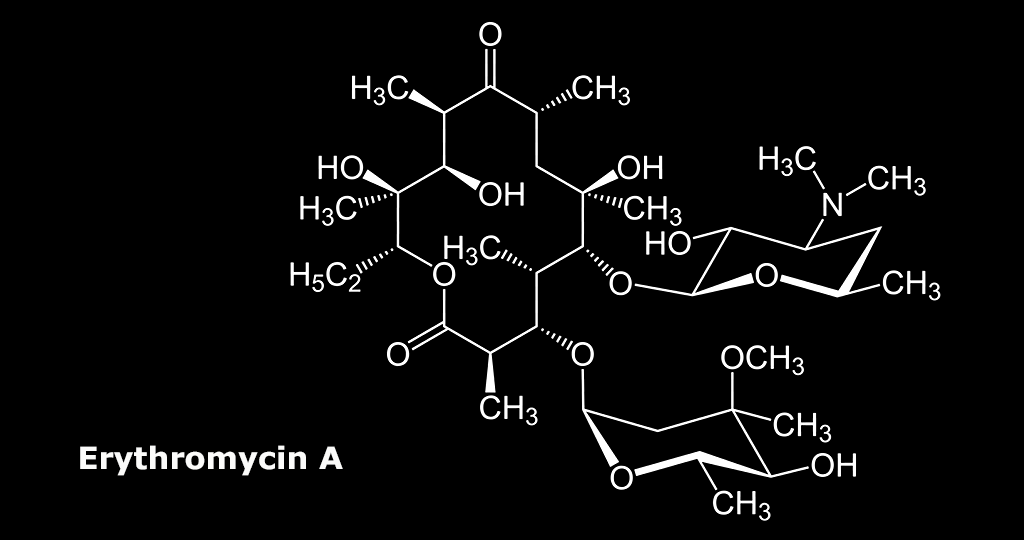
Makrolid-Antibiotika wie das Erythromycin gehören neben Tetracycline und Betalactam-Antiobiotika zu den am häufigsten verordneten Antibiotika in der ambulanten Praxis.
Makrolide stellen eine große Familie von Proteinsynthesehemmern dar, die aufgrund ihrer vielseitigen Anwendbarkeit in der Humanmedizin von großem klinischem Interesse sind, sie wirken als Antibiotika, indem sie an die bakterielle 50S-ribosomale Untereinheit binden und die Proteinsynthese stören. Die hohe Affinität von Makroliden zu bakteriellen Ribosomen sowie die hochkonservierte Struktur von Ribosomen über praktisch alle Bakterienarten hinweg stimmen mit ihrer Breitbandaktivität überein. Seit der Entdeckung des Vorläufer der Makrolid-Antibiotika Erythromycin im Jahr 1950 wurden viele Derivate synthetisiert, was zu Verbindungen mit besserer Bioverfügbarkeit und Säurestabilität sowie verbesserter Pharmakokinetik führte.
Diese Bemühungen führten zur zweiten Generation von Makroliden, einschließlich bekannter Mitglieder wie Azithromycin und Clarithromycin.
Schließlich hat man eine dritte Generation von Makroliden entwickelt, die eine verbesserte Aktivität gegen viele makrolidresistente Stämme zeigen, um der zunehmenden Antibiotikaresistenz entgegenzuwirken. Diese Verbesserungen gingen jedoch mit schwerwiegenden Nebenwirkungen einher, die zu Enttäuschungen führten und dazu führten, dass viele Forscher die Arbeit an Makrolidderivaten einstellten.
Im Gegensatz dazu führte ein kürzlich veröffentlichter Durchbruch eine neue chemische Plattform für die Synthese und Entdeckung einer breiten Palette verschiedener Makrolid-Antibiotika ein. Diese Revolution der chemischen Synthese hat in Kombination mit der Verringerung der Nebenwirkungen zu einer Makrolid-Renaissance geführt und die Hoffnung auf neuartige und sichere Therapeutika zur Bekämpfung schwerer Infektionskrankheiten beim Menschen erhöht.
Pharmakologie
Die diversen Wirkstoffe aus der Familie der Makrolide unterscheiden sich in ihrer Affinität zum Cytochrom-P450-Isoenzym 3A4. Aufgrund ihres ähnlichen Wirkungsspektrums und ihrer Wirksamkeit gegen atypische Erreger stellen Makrolid-Antibiotika (Erythromycin & Co.) und Tetracycline in der Antibiotika-Therapie bei vielen Indikationen eine gegenseitige Alternative dar.
Vertreter der Makrolid-Antibiotika sind Erythromycin (der älteste), Clarithromycin, Roxthromycin, Azithromycin und Josamycin. Ältester Vertreter ist das Erythromycyn, das im Jahr 1949 vom Pharmaunternehmen Lilly (dort die Wissenschaftern Abelardo Aguilar und J. M. McGuire mit seinem Team) entdeckt und als das Stoffwechselprodukt von Streptomyces erythreus isoliert wurde. Erythromycin gilt als die Leitsubstanz der Makrolid-Antibiotika, wurde aber von Clarithromycin, Azithromycin, Roxthromycin und Josamycin zunehmend verdrängt.
Makrolid-Antibiotika sind strukturell durch einen 12- bis 16-gliedrigen makrocylischen Lactonring mit einem glykosidisch gebundenen Aminozucker gekennzeichnet. Sie greifen an der 50s-Untereinheit der 70s-Ribosomen von Bakterien in die Proteinbiosynthese während des dritten Schritts der Elongationsphase der Polypeptidkette am Ribosom ein und binden an die Untereinheit und blockieren damit die Translokation der Peptidyl-t-RNA von der Akzeptorstelle zur Donorstelle. Die Proteinbiosynthese der Bakterien kommt zum Erliegen und in der Folge kommt es zur Bakteriostase.
Die orale Bioverfügbarkeit der Makrolid-Antibiotika ist mittelmäßig, beim Erythromycin und seinen Derivaten schwankt sie stark in Abhängigkeit von der Nahrungsaufnahme und von der jeweils eingesetzten Verbindung. Aufgrund der guten Gewebegängigkeit und der Fähigkeit, sich intrazellulär anzureichern, haben Makrolide relativ niedrige Plasmaspiegel.
Längere Plasmahalbwertszeiten erlauben bei Roxithromycin und Azithromycin eine einmalige Dosierung, die Gewebehalbwertszeit des Azithromycins beträgt 2 bis 4 Tage und ermöglicht bei vielen Erkrankungen die kurzfristige Behandlung von 3 Tagen. Die verbesserten pharmakokinetischen Eigenschaften und reduzierte Einnahmehäufigkeit sind Vorteile neuerer Makrolide.
Gegen welche Erreger Makrolid-Antibiotika Wirkung zeigen
Makrolid-Antibiotika wirken primär auf grampositive Bakterien wie Staphylokokken oder Streptokokken, Bei den gramnegativen Bakterien gehören die Gattungen Neisseria, Haemophilus, Bordetella, Legionella und Brucella dazu. Weiter wirken sie gegen einige Anaerobier und gegen schraubenförmige Bakterien wie Treponemen, Borrelien und Campylobacter sowie zellwandlose Bakterien wie Mykoplasmen, Chlamydien und Rickettsien.
Wirkung und Resistenzen
Enterobakterien hingegen sind nicht gegen Makrolide empfindlich. Das Spektrum beinhaltet somit häufige Erreger von bakteriellen Infektionen der Atemwege und der Haut sowie (sexuell übertragbare) Infektionen des Urogenitaltraktes.
Makrolid-Antibiotika können aufgrund ihres Wirkspektrums und des strukturellen Unterschiedes als Ersatz für Betalactam-Antibiotika bei einer bestehenden Penicillinallergie des Patienten herangezogen werden. Die antimikrobiellen Wirkstoffe zählen jedenfalls neben Betalactam-Antibiotika zu den bestverträglichsten Antibiotika überhaupt.
Die häufigsten Nebenwirkungen der Makrolide sind in 5% der Fälle gastrointestinale Störungen wie Übelkeit, Erbrechen, Bauchschmerzen oder Durchfall. Makrolid-Antibiotika sollten nicht zusammen mit Terfenadin oder Astemizol angewendet werden.
Da Makrolide vor allem im niedergelassenen Bereich zur Antibiotika-Therapie zum Einsatz kommt, spielt die Resistenzsituation bei der Auswahl eine wichtige Rolle. Im Grunde genommen ist durch zunehmende Resistenzen das Erreger-Spektrum heutzutage sehr eingeschränkt – vor allem gegenüber Erythromycin.
Besonderer Stellenwert bei Erkrankungen der Atemwege
Auch heute haben Makrolid-Antibiotika besonders bei Infektionen des Respirationstraktes sowie bei Vorliegen von so genannten atypischen Erregern wie Chlamydophila, Mykoplasmen und Legionellen nach wie vor einen hohen Stellenwert. Sie sind gute verträglich, sind sicher beim Einsatz bei Kindern sowie in der Schwangerschaft, haben eine gute Gewebsgängigkeit und zeigen teilweise antiinflammatorische Aktivitäten.
Makrolide gehen in die Muttermilch, wobei die Auswirkungen beträchtlich sein können. Die Verordnung von Makrolid-Antibiotika an die Mutter in den ersten 13 Tagen nach der Geburt des Kindes war mit einer erhöhten Rate von Pylorusstenosen bei ihrem Kind assoziiert. So erhöhte sich in einer Studie (publiziert 2014) die Zahl der später operativ korrigierten Pylorusstenosen um 24,4 Fälle pro 1000 Kinder. Experten empfehlen daher, auf die Verordnung von Makroliden in den ersten Lebenswochen eines Säuglings zu verzichten.
Immunmodulation durch Makrolide: Therapeutisches Potenzial für die Intensivpflege in der Corona-Pandemie
Kritische Erkrankungen sind mit einer Dysregulation des Immunsystems verbunden, die durch gleichzeitige Hyperinflammation und Immunsuppression gekennzeichnet ist. Eine Hyperinflammation kann zu Kollateralgewebeschäden und Organversagen führen, während die Immunsuppression mit der Anfälligkeit für Sekundärinfektionen und der Reaktivierung latenter Viren in Verbindung gebracht wurde.
Makrolide sind eine Klasse von bakteriostatischen Antibiotika, die im Grunde genommen auf der Intensivstation zur Bekämpfung von Infektionen oder zur Linderung der gastrointestinalen Dysmotilität eingesetzt werden.
Sie haben jedoch auch starke und weitreichende immunmodulatorische Eigenschaften, die das Potenzial haben könnten, die Dysregulation des Immunsystems bei kritisch kranken Patienten zu korrigieren. Und zwar ohne die entscheidende antimikrobielle Abwehr zu beeinträchtigen. Dies kann bei verschiedenen akuten Erkrankungen in der Intensivpflege relevant sind.
Literatur:
Reijnders TDY, Saris A, Schultz MJ, van der Poll T. Immunomodulation by macrolides: therapeutic potential for critical care. Lancet Respir Med. 2020;8(6):619‐630. doi:10.1016/S2213-2600(20)30080-1
Dinos GP. The macrolide antibiotic renaissance. Br J Pharmacol. 2017;174(18):2967‐2983. doi:10.1111/bph.13936
Brittain DC. Erythromycin. Med Clin North Am. 1987;71(6):1147‐1154. doi:10.1016/s0025-7125(16)30802-1