Guselkumab – Handelsname TREMFYA ® – ist das erste zugelassene Biologikum, das sich selektiv gegen Interleukin (IL)-23 richtet.
Die Europäische Kommission das Medikament TREMFYA ® mit dem Wirkstoff Guselkumab für die Therapie von Erwachsenen mit mittelschwerer bis schwerer Plaque-Psoriasis genehmigt, die für eine systemische Therapie in Frage kommen.[1] Guselkumab ist das erste Biologikum, das selektiv Interleukin (IL)-23 blockt, den maßgeblich entzündungsfördernden Botenstoff in der Immunreaktion bei Psoriasis.[2],[3],[4],[5]
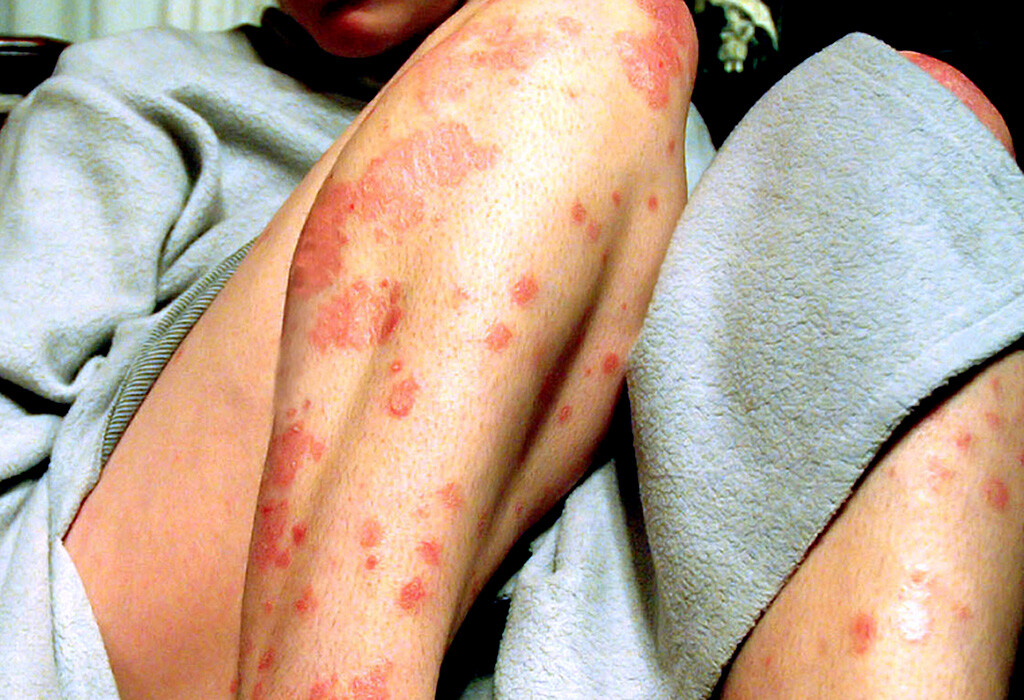
Guselkumab für Menschen mit Plaque-Psoriasis
Guselkumab ist eine subkutan verabreichte, vom Patienten (nach entsprechendem Training) selbst injizierbare Psoriasis-Therapie. Zu Behandlungsbeginn werden zwei Startdosen in den Wochen Null und Vier injiziert, gefolgt von einer Erhaltungsdosis alle acht Wochen (q8w).[3],[4]
Die Zulassung durch die EU-Kommission basiert auf Daten aus drei klinischen Phase-III-Studien. Die VOYAGE 1 und VOYAGE 2 Studien verglichen Guselkumab mit Placebo und Adalimumab und zeigten nach nur 16 Wochen eine signifikante Verbesserung des Hautbildes mit mindestens 90-prozentiger Verbesserung entsprechend PASI 90 (Psoriasis Area and Severity Index) bei 73,3 % bzw. 70,0 % der mit Guselkumab behandelten Patienten im Vergleich zu 49,7 % bzw. 46,8 % der mit Adalimumab behandelten Patienten (P<0.001).[2],[3]
Die NAVIGATE Studie untersuchte Patienten, die auf die Behandlung mit Ustekinumab bis Woche 16 weder mit ‚erscheinungsfrei‘ oder ‚minimalem Erscheinungsbild‘ (Investigator’s Global Assessment [IGA] Score von 0 oder 1) ansprachen und daraufhin randomisiert entweder auf Guselkumab umgestellt wurden, oder weiterhin Ustekinumab erhielten.[4] Die Guselkumab-Gruppe profitierte maßgeblich von der Umstellung mit einer signifikant höheren durchschnittlichen Anzahl von Patienten, die einen IGA-Score von 0 oder 1 und eine Verbesserung um mindestens 2 Stufen von Woche 28 bis Woche 40 (relativ zu Woche 16) im Vergleich zur Ustekinumab-Gruppe (1.5 vs. 0.7; P<0.001) aufwiesen.[4]
Während des klinischen Entwicklungsprogramms für Guselkumab bei Psoriasis gab es keine eindeutigen Anzeichen für ein erhöhtes Risiko von Malignomen, schwerwiegenden kardiovaskulären Ereignissen oder schweren Infektionen, einschließlich Tuberkulose und reaktivierter latenter Tuberkulose.[2],[3],[4] Bei mindestens 5 % der mit Guselkumab behandelten Patienten traten in den ersten 16 Wochen der Studien VOYAGE 1 und 2 die folgenden Nebenwirkungen auf: Nasopharyngitis, Infektionen der oberen Atemwege, Erytheme an der Injektionsstelle, Kopfschmerzen, Arthralgie, Juckreiz und Rückenschmerzen. Die Art der berichteten Nebenwirkungen blieb im Verlauf von 48 Behandlungswochen generell konsistent.[2],[3]
Die Genehmigung für die Marktzulassung folgt auf eine positive Stellungnahme des Ausschusses für Humanarzneimittel (Committee for Medicinal Products for Human Use, CHMP) der Europäischen Arzneimittel-Agentur EMA vom 14. September 2017.[6] Diese Zulassung ermöglicht das Inverkehrbringen von TREMFYA ® (Guselkumab) in allen 28 Mitgliedstaaten der Europäischen Union sowie in den Ländern des Europäischen Wirtschaftsraums (Norwegen, Island und Liechtenstein).
Quellen:
1. European Commission: Tremfya (guselkumab). Available at: http://ec.europa.eu/health/documents/community-register/html/h1234.htm. Accessed: November 2017.
2. Blauvelt A and Papp K.A et al. J Am Acad Dermatol 2017;76(3):405-17.
3. Reich K and Armstrong A.W et al. J Am Acad Dermatol 2017;76(3):418-31.
4. Langley R.G and Tsai T.F et al. Br J Dermatol 2017 [Epub vor Drucklegung].
5. Bachelez H. The Lancet 2017;390:208-10.
6. Europäische Arzneimittel-Agentur. 2017. Verfügbar unter: http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/human/medicines/004271/smops/Positive/human_smop_001193.jsp&mid=WC0b01ac058001d127&source=homeMedSearch&category=human. Zugriff im November 2017.
7. US Food and Drug Administration. 2017. Verfügbar unter: https://www.fda.gov/drugs/developmentapprovalprocess/druginnovation/ucm537040.htm . Zugriff im November 2017.
8. Griffiths C.E and Papp K.A et al. 26th European Academy of Dermatology and Venereology Congress (EADV 2017) 13. – 17. Sept, 2017; Genf, Schweiz;D3T01.1I.
9. ClinicalTrials.gov. Verfügbar unter: clinicaltrials.gov/ct2/show/NCT03158285. Zugriff im November 2017.
10. ClinicalTrials.gov. Verfügbar unter: clinicaltrials.gov/ct2/show/NCT03090100. Zugriff im November 2017.
11. National Institute of Arthritis and Musculoskeletal and Skin Disorders. NIH Medline Plus 2003;12(1):20-1.
12. US Food and Drug Administration. 2016. Verfügbar unter: https://www.fda.gov/downloads/ForIndustry/UserFees/PrescriptionDrugUserFee/UCM529856.pdf . Zugriff im November 2017.
13. Rapp S.R and Feldman S.R et al. J Am Acad Dermatol 1999;41(3):401-7.
14. Nijsten T and Wakkee M J Invest Dermatol 2009;129(7):1601-3.
15. National Psoriasis Foundation. Verfügbar unter: psoriasis.org/about-psoriasis/related-conditions. Zugriff im November 2017.
16. World Health Organization. 2016. Verfügbar unter: apps.who.int/iris/bitstream/10665/204417/1/9789241565189_eng.pdf. Zugriff im November 2017.