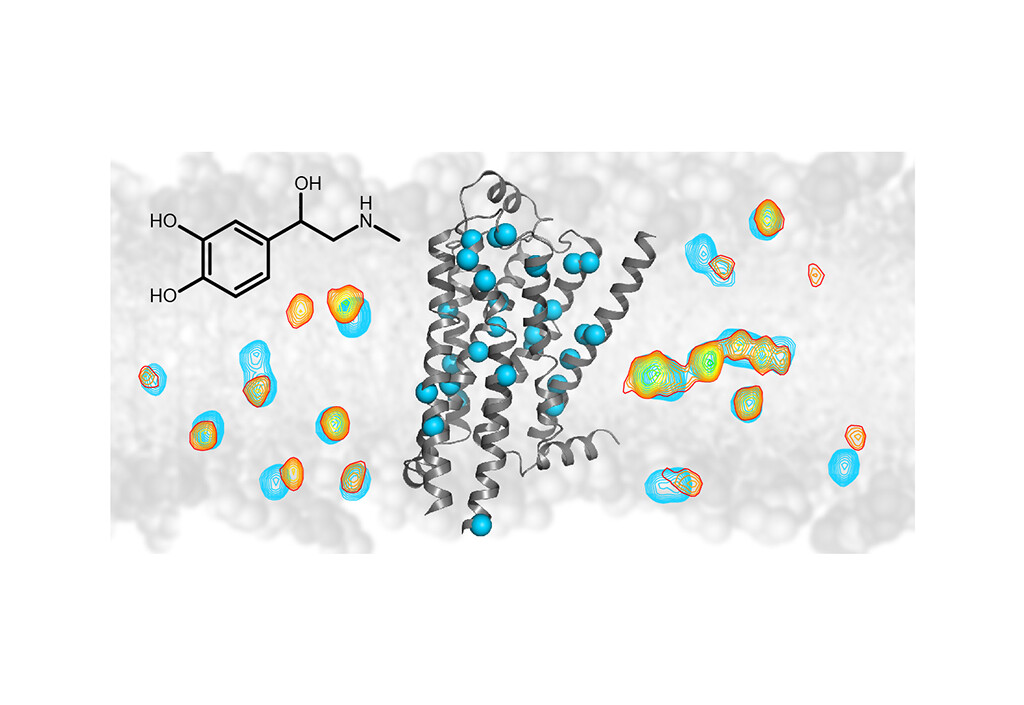
Etwa 30% aller Wirkstoffe – wie Betablocker und Antidepressiva – wirken über bestimmte Membranproteine, den sogenannten G-Protein-gekoppelte-Rezeptoren.
In Zusammenarbeit mit Forschern des Paul-Scherrer-Instituts hat das Team von Prof. Stephan Grzesiek vom Biozentrum der Universität Basel nun im Detail aufgeklärt, wie sich die Struktur von solchen G-Protein-gekoppelte-Rezeptoren bei Bindung der Wirkstoffe verändert und so die Signalübertragung ins Zellinnere steuert. Die Studie wurde unlängst in «Nature» veröffentlicht.
Wie G-Protein-gekoppelte-Rezeptoren Signale ins Innere einer Zelle übertragen
Eine Vielzahl von Medikamenten wie Betablocker gegen Bluthochdruck oder Arzneistoffe zur Behandlung von Allergien, Krebs, Parkinson oder HIV binden an Proteine auf der Zelloberfläche, die zur Familie der G-Protein-gekoppelte-Rezeptoren gehören. Binden Arzneistoffe an solche G-Protein-gekoppelte-Rezeptoren, so leiten diese ein Signal ins Zellinnere weiter. Obwohl bereits zahlreiche Strukturen dieser G-Protein-gekoppelte-Rezeptoren bekannt sind, war bis jetzt nicht klar, wie die Signale ins Innere einer Zelle übertragen werden.
Um die Art und Weise der Signalübertragung besser zu verstehen, hat das Forscherteam einen bestimmten Rezeptor – den sogenannten Beta-1-Adrenorezeptor – genauer untersucht. Mithilfe der Kernmagnetresonanzspektroskopie (NMR) konnten sie verfolgen, wie die Struktur des Rezeptors auf verschiedene Wirkstoffe reagiert und erhielten damit ganz neue, detaillierte Einblicke in die Funktionsweise der gesamten Familie der G-Protein-gekoppelte-Rezeptoren.
Strukturänderungen geben Details über Rezeptorfunktion preis
Der Beta-1-Adrenorezeptor ist ein Protein, das in der Membran von Herzzellen zu finden ist. Es fungiert als Übersetzer, denn durch das Andocken von Molekülen an der Zelloberfläche des Rezeptors werden Proteine im Zellinneren aktiviert. So löst zum Beispiel das Hormon Noradrenalin eine Signalkaskade aus, die schliesslich zum Anstieg der Herzfrequenz und des Blutdrucks führt. Betablocker wirken dem entgegen, indem sie das Hormon daran hindern, an den Beta-1-Adrenorezeptor anzudocken. Genaue Details, wie die Bindung von Molekülen an den Rezeptor dessen Struktur verändert und so die Signalübertragung moduliert, waren bislang jedoch unklar.
«Wir haben mittels hochauflösender NMR-Spektroskopie die strukturellen Veränderungen des Beta-1-Adrenorezeptor nach Bindung verschiedener Wirkstoffen analysiert», erklärt Shin Isogai, Erstautor der Studie. «So konnten wir beobachten, wie der Rezeptor seinen Bindungspartner erkennt, dessen chemische Struktur interpretiert und durch die Änderung seiner eigenen Struktur diese Information anschliessend ins Zellinnere weiterleitet. Diese Erkenntnisse über die Funktionsweise des Beta-1-Adrenorezeptors lassen sich auf die ganze Familie der pharmakologisch bedeutsamen G-Protein-gekoppelte-Rezeptoren übertragen.»
Wirksamkeit von Arzneistoffen lässt sich vorhersagen
Durch die NMR-Analyse der Signale aus den Atomkernen konnten die Forscher feststellen, wie tief ein Wirkstoff in den Rezeptor eindringt, dabei einzelne Proteinteile beiseite schiebt, und wie dieses mechanische Signal ins Zellinnere übertragen wird. Dadurch konnten wichtige mechanische Verknüpfungen innerhalb der Rezeptorstruktur identifiziert werden, die für die Signalübertragung eine Rolle spielen. Die NMR-Daten geben auch ein direktes Mass für die Bindungsstärke der verschiedenen Wirkstoffe und für ihr Potenzial in der Zelle eine Antwort auszulösen. Es war sogar möglich, eine solche Antwort direkt beim Binden eines intrazellulären Signalproteins an den aktivierten Rezeptor zu verfolgen.
Fazit: Der Beta-1-Adrenorezeptor gehört zur Familie der sogenannten G-Protein-gekoppelte-Rezeptoren. Da diese allesamt vergleichbare Mechanismen haben, lassen sich die neuen Ergebnisse der Forschenden auf diese ganze Rezeptorfamilie übertragen.
G-Protein-gekoppelte-Rezeptoren wiederum sind für die Wirkweise von rund 30 Prozent aller neu zugelassenen Medikamente verantwortlich und daher von grosser Bedeutung in der Medizin.
„Nur das kombinierte Expertenwissen der Forschenden am PSI und am Biozentrum Basel hat dieses Forschungsergebnis möglich gemacht“, sind sich Dmitry Veprintsev und Gebhard Schertler vom PSI einig. Ihr Team hat jahrelange Erfahrung in der Forschung mit G-Protein-gekoppelte-Rezeptoren. So entwickelten sie eine stabilisierte Version vom Beta-1-Adrenorezeptor, was die hohe Qualität der NMR-Messungen ermöglichte, die am Biozentrum der Universität Basel stattfanden.
«Da G-Protein-gekoppelte-Rezeptoren extrem schwierig zu untersuchen sind, freut es uns umso mehr, dass wir nun erstmals solche Einzelheiten aufdecken konnten. Viele Wissenschaftler treibt das schon mehr als ein Jahrzehnt um», betont Isogai. «Wir werden die Technik nun zur Erforschung der Rolle einzelner Aminosäuren in der Signalübertragung sowie anderer Rezeptoren verwenden.» Zukünftig könnte die NMR-Methode auch bei der Entwicklung und Testen neuer Arzneimittel zum Einsatz kommen.