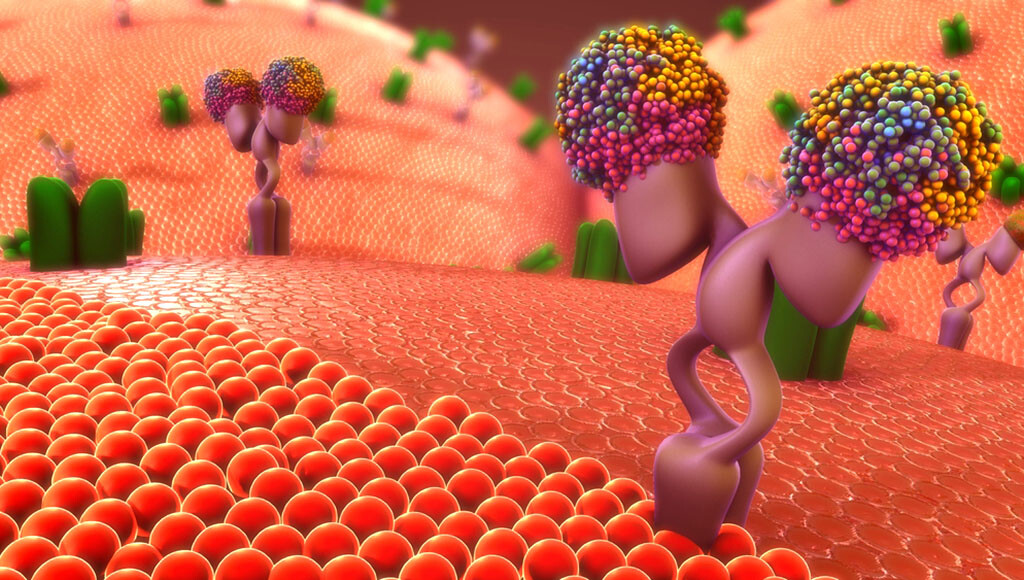
Bei vielen Vorgängen in unserem Körper empfangen G Protein gekoppelte Rezeptoren (GPCR) auf der Zelloberfläche verschiedene Signale und leiten diese weiter.
Im Grunde genommen wirken körpereigene Botenstoffe sowie Medikamente über G Protein gekoppelte Rezeptoren (GPCR) auf der Oberfläche der Zellen. Wissenschaftler am Berlin Institute of Health (BIH) konnten nun erstmals die initialen Schritte beobachten, wie der Rezeptor auf der Zellinnenseite so genannte G Proteine bindet. Und wie er so das Signal gezielt in die Zelle überträgt. Das gelang ihnen, indem sie ihre Expertisen in der Strukturbiologie bzw. in high-performance Computermethoden kombinierten. Ihre Erkenntnisse über haben die Wissenschaftler in der Zeitschrift Cell veröffentlicht. Beide BIH Visiting Professoren werden von der Stiftung Charité gefördert.
G Protein gekoppelte Rezeptoren (GPCR) spielen als Signalsempfänger im Körper eine entscheidende Rolle
Beispielsweise wandeln lichtempfindliche Rezeptoren das Licht in der Retina unseres Auges in körpereigene Signale um. Diese werden dann im Gehirn zu dem zusammengefügt, was wir schließlich sehen. Das Stresshormon Adrenalin signalisiert Gefahr und sorgt für erhöhte Pulsschlag- und Atemfrequenz. Die Botenstoffe wie Serotonin sorgen für die Aktivierung von Nervenzellen in bestimmten Gehirnarealen, was zum Beispiel Glücksgefühle auslöst. Bei all den beschreiben Vorgängen spielen spezielle Antennen auf der Zelloberfläche eine alles entscheidende Rolle. Diese sogenannten G Protein gekoppelte Rezeptoren (GPCR) empfangen die Signale, leiten sie und lösen damit eine bestimmte Reaktion im Körper aus. Wobei G Protein gekoppelte Rezeptoren schon sehr lang bekannt sind und die Forschung diese auch sehr genau untersucht hat.
Computersimulation krankheitsrelevanter Eiweißmoleküle
Peter Hildebrand, Professur für biophysikalische Computersimulationen an der medizinischen Fakultät der Universität Leipzig, beschäftigt sich mit der Computersimulation krankheitsrelevanter Eiweißmoleküle im Körper. „Wir interessieren uns seit vielen Jahren dafür, was passiert, nachdem das Signal auf seinen Rezeptor an der Zelloberfläche gestoßen ist“, erzählt Peter Hildebrand, der am BIH Visiting Professor ist.
„Wir wollen wissen, wie der Rezeptor das Signal in die Zelle hinein reicht und wie es dann innerhalb der Zelle weiter geht: Diese ersten Schritte entscheiden, welches Programm in der Zelle im Anschluss abläuft und welche Antwort die Zelle darauf liefert.“
Für Antworten auf solche Fragen hat der Strukturbiologe Brian Kobilka der Universität Stanford 2012 den Nobelpreis für Chemie erhalten. “Und deshalb ist es für uns auch so ein großes Glück, dass wir mit Brian Kobilka ,der am BIH als BIH Einstein Visiting Professor tätig ist, hier in Berlin zusammenarbeiten können“, freut sich Hildebrand.
Schnappschüsse von Rezeptoren im Moment der Bindung
„Brian Kobilka hat Schnappschüsse von Rezeptoren im Moment der Bindung des von außen kommenden Botenstoffs und ebenfalls im Moment der Bindung an die G Proteine innerhalb der Zelle aufgenommen“, erklärt Hildebrand. „Wir konnten die Bewegungen dieser Molekülen in ihrer natürlichen Umgebung simulieren.“
Der Biophysiker Hildebrand tat sich daraufhin in Berlin mit dem Strukturbiologen und Mediziner Kobilka zusammen. „Wir wollten genau verstehen, was unter der Zelloberfläche bei der Signalübertragung passiert. Die entscheidenden Bewegungen laufen dabei in sehr kurzer Zeit, also wenigen Bruchteilen von Sekunden ab“, beschreibt Hildebrand das Problem.
„Wir konnten nur zusammen herausfinden, wovon es abhängt, ob ein Signal weitergereicht wird. Und ob es in die eine oder in die andere Richtung weitergeleitet wird.“ Dazu haben sie die Bewegungen des Rezeptors am Computer simuliert und anschließend im Labor mit strukturbiologischen Methoden überprüft, ob die Simulation die Vorgänge korrekt widerspiegelte.
Ultraschnelle mikroskopische Bewegungen beobachtet
Kobilka und Hildebrand konnten nun erstmals die mikroskopisch kleinen ultraschnellen Bewegungen beobachten. Diese entscheiden zu einem wesentlichen Teil darüber, welche Wirkung ein natürliches oder körpereigenes Signal entfaltet. Auch ein Drittel der Medikamente wirkt über diese Rezeptoren, etwa Herzmedikamente, Psychopharmaka oder Schmerzmittel.
„Dabei kommt es auf die speziellen Bewegungen an, die das Medikament bewirkt, wenn es an den Rezeptor bindet“, erklärt Hildebrand. „Die jetzt veröffentlichten Erkenntnisse sind ein wichtiger Schritt, um in Zukunft abzuschätzen zu können, ob ein Medikament Nebenwirkungen hervorrufen wird, weil es nicht nur einen, sondern mehrere oder den falschen Signalweg in der Zelle aktiviert,“ ordnet Hildebrand die aktuelle Veröffentlichung ein.
Literatur:
Liu et al. Structural Insights into the Process of GPCR-G Protein Complex Formation. Cell, Volume 177, Issue 5, 16 May 2019, Pages 1232-1242.e11, https://doi.org/10.1016/j.cell.2019.04.021
Quelle: Berliner Institut für Gesundheitsforschung / Berlin Institute of Health (BIH)