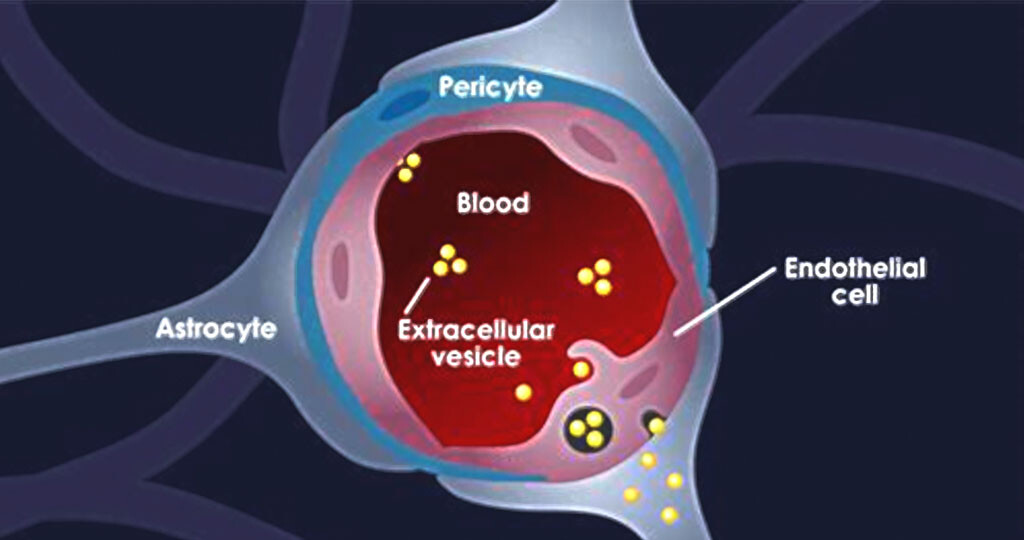
Brustkrebs gibt Exosomen ab, die Zellen in der Blut-Hirn-Schranke dazu bringen, diese Vesikel aufzunehmen und so die Entwicklung von Metastasen im Gehirn fördern.
Im Grunde genommen sind Exosomen etwa 30 bis 90 nm große Vesikel, die von einer Zelle an die Umgebung abgegeben werden. Beispielsweise können Lymphzellen, Blutplättchen, Mastzellen, dendritischen Zellen, Nervenzellen, Astrozyten sowie auch Krebszellen diese bilden. Die Vesikel beinhalten unter anderem Nukleinsäuren und Proteine in wechselnder Zusammensetzung. Sie dienen als Transportvehikel und zur Ausschleusung von Zellbestandteilen und spielen möglicherweise auch bei der erworbenen Immunität eine Rolle. In den letzten Jahren untersuchte die Forschung die Exosomen im Zusammenhang mit Therapien von Autoimmunerkrankungen und Krebs. Nun beschreibt eine aktuelle Studie des BOSTON CHILDREN’S HOSPITAL, wie Exosomen, die von Brustkrebs-Zellen freigesetzt werden, Zellen in der Blut-Hirn-Schranke dazu bringen, sie aufzunehmen und in Folge die Entwicklung von Metastasen im Gehirn zu begünstigen.
Metastasen im Gehirn sind bei Brustkrebs besonders gefährlich
Bei metastasierendem Brustkrebs treten normalerweise Metastasen in den Knochen, der Lunge und im Gehirn auf. Wobei die Metastasen im Gehirn besonders gefährlich sind. Denn viele erkrankte Frauen überleben weniger als einem Jahr nach dieser speziellen Diagnose. Doch wie kann der Krebs die Blut-Hirn-Schranke überwinden und wie kann man das verhindern?
Um diese Fragen zu beantworten, untersuchten die Forscherinnen Golnaz Morad und Marsha Moses Moses im Lab eine eingehend die Exosomen der Brustkrebs-Zellen. Dabei konnten sie den Mechanismus identifizieren, mit dem die Exosomen die Blut-Hirn-Schranke passieren konnten. Diese ‚Nische‘ ermöglichte es schließlich den Brustkrebs-Zellen, Metastasen im Gehirn zu bilden. Dazu nutzen die Exosomen einen Standard-Bioweg, die sogenannte Transzytose. In Folge nahmen die Zellen der Blut-Hirn-Schranke einfach die Exosomen auf. Dann brachten sie diese ins Gehirn hinein und gaben sie wie viele trojanische Pferde ins Gehirngewebe ab.
Prozess umkehren
Nachdem die Forscherinnen des Moses Lab herausgefunden hatten, wie die Exosomen das Gehirn erreichten, wollen sie den Spieß nun umdrehen. Mithilfe der Exosomen beziehungsweise synthetischer Versionen davon sollen statt Krebszellen Krebsmedikamente ans Ziel gebracht werden.
Literatur:
Golnaz MoradChristopher V. CarmanElliott J. HagedornJulie R. PerlinLeonard I. ZonNur MustafaogluTae-Eun ParkDonald E. IngberCassandra C. DaisyMarsha A. Moses. Tumor-Derived Extracellular Vesicles Breach the Intact Blood–Brain Barrier via Transcytosis. ACS Nano2019. Publication Date: September 3, 2019. https://doi.org/10.1021/acsnano.9b04397.
Quelle: BOSTON CHILDREN’S HOSPITAL