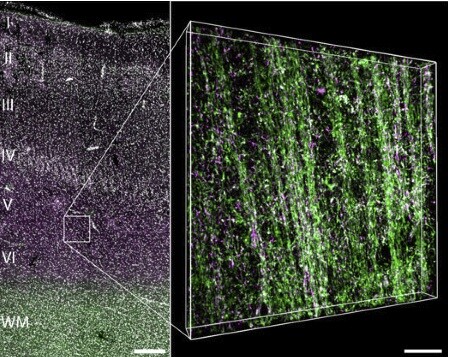
Zur Epilepsie auf molekularer Ebene haben Forscher den Zusammenhang zwischen fehlgebildeter Hirnrinde und der neurologischen Erkrankung erforscht.
Die Frage, warum eine strukturelle Unregelmäßigkeit im Schläfenlappen des Menschen das Potenzial für epileptische Anfälle erhöht, beschäftigt Epilepsie-Experten schon seit Langem. Herkömmliche Antiepileptika unterdrücken das übermäßige Abfeuern von Neuronen während der Anfälle. Bei arzneimittelresistenten Patienten weist ein Therapieversagen auf alternativen wichtigen epileptogenen Auslöser hin. Im Grunde genommen weisen zwei Epilepsie-assoziierte Pathologien Myelinmängel in anfallsbedingten Hirnregionen hin. Das sind die fokale kortikale Dysplasie IIB (FCD) sowie kortikale Knollen im Tuberous Sclerosis Complex (TSC).
Pathologische Prozesse im Gewebe als Epilepsie-Ursache
Unlängst beschrieben Freiburger Forscher die pathologischen Prozesse im Gewebe bei einer Entwicklungsstörung der Großhirnrinde. Dabei zeigten sich bei etwa 25 Prozent der auf bestimmte Bereiche begrenzten Epilepsien sogenannte „fokale kortikale Dysplasien“. Dies bezeichnet die krankhaften Veränderungen der Hirnrinde. Schließlich sprechen Patienten mit diesen Dysplasien oft nicht auf die Behandlung mit Antiepileptika an.
Der bislang wirkungsvollste therapeutische Ansatz ist, die betroffenen Areale zu entfernen. Denn nach einer Operation kommen in der Regel keine epileptischen Anfälle mehr vor. Bisher konnten Forscher jedoch nur vermuten, welche molekularen Zusammenhänge zwischen der abweichenden Hirnrindenstruktur und dem Auftreten von Epilepsie bestehen.
Hirnrindengewebe
Um zu einem detaillierten Verständnis zu gelangen, hatten die Wissenschaftler verglichen, welche Gene bei fehlgebildetem Hirnrindengewebe und epileptischem, nicht fehlgebildeten Hirnrindengewebe exprimiert sind. Dazu nutzten die Forscher so genannte Microarrays, einer Chiptechnologie, die ursprünglich aus der Halbleiterindustrie stammt. Auf diese Weise konnte man zeigen, dass vor allem Faktoren, die für die Bildung von Myelin verantwortlich sind, im kranken Gewebe weniger stark ausgeprägt sind. Bei Myelin handelt es sich um eine die Nervenzellen elektrisch abschirmende Schicht.
Zusätzliche Analysen zeigten, dass die Struktur dieser Schicht aufgebrochen und durcheinander gebracht erscheint. Dadurch könnte die Leitung der Reize in der betroffenen Hirnregion nicht unerheblich eingeschränkt sein.
Möglicherweise lässt sich die Neigung zu Epilepsie bei der untersuchten Fehlbildung auf eine dadurch entstandene elektrische Überreizbarkeit jener Nervenfaserumhüllung zurückführen, meinen die Forscher. Zukünftig will man deswegen erforschen, was im fehlgebildeten Gewebe bei der Entwicklung von Myelin genau passiert.
Literatur:
C. Donkels, D. Pfeifer, P. Janz, S. Huber, J. Nakagawa, M. Prinz, A. Schulze-Bonhage, A. Weyerbrock, J. Zentner, C. Haas (2016). Whole Transciptome Screening Reveals Myelination Deficits in Dysplastic Human Temporal Neocortex. In: Cerebral Cortex., pp. 1-15.
Scholl et al. Impaired oligodendroglial turnover is associated with myelin pathology in focal cortical dysplasia and tuberous sclerosis complex. Brain Pathol. 2017 Nov;27(6):770-780. doi: 10.1111/bpa.12452. Epub 2017 Feb 9.
Quelle: Exzellenzcluster BrainLinks-BrainTools der Albert-Ludwigs-Universität Freiburg