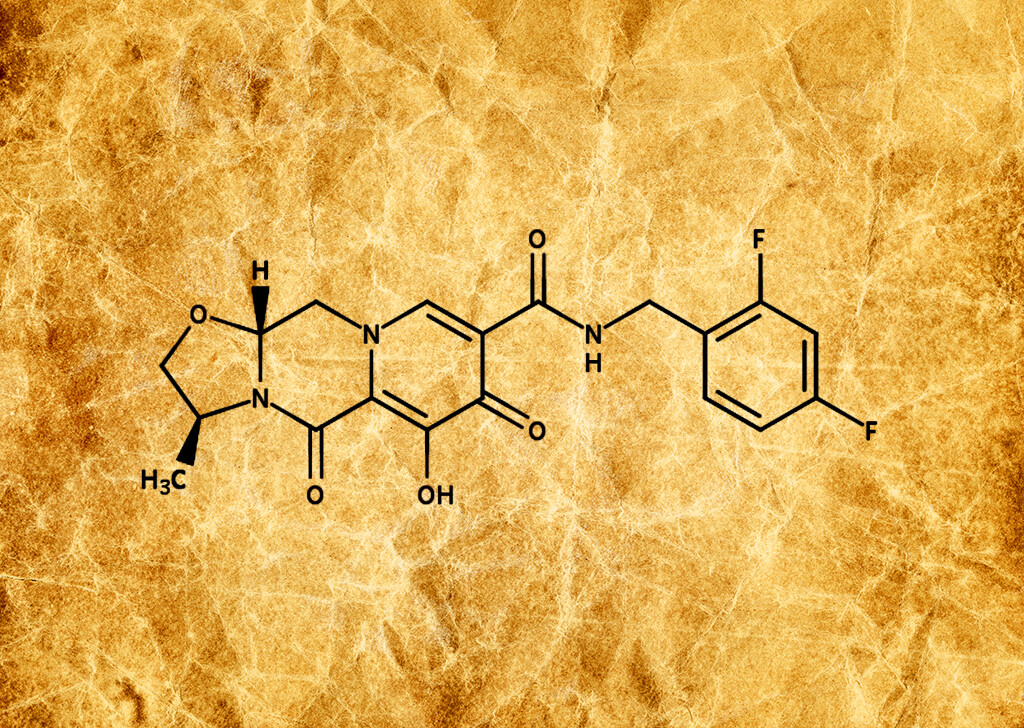
Erste positive Ergebnisse einer Phase II-Studie zur Prävention von HIV mit lang wirksamem, injizierbaren Cabotegravir wurden jetzt bekannt gegeben.
Weltweit leben mehr als 36 Millionen Menschen mit einer HIV-Infektion, und trotz großer Fortschritte im Kampf gegen HIV steigt die Zahl an Infektionen in manchen Teilen der Welt immer noch. Nun wurden positive Ergebnisse zum neuen Wirkstoff Cabotegravir in einer 41-wöchigen Phase IIa-Studie ECLAIR präsentiert. In der ECLAIR-Studie wurden Sicherheit, Verträglichkeit, Dosierung und Zufriedenheit mit der experimentellen, lang wirksamen, injizierbaren Formulierung von Cabotegravir als Monotherapie für die Präexpositionsprophylaxe (PrEP) bei nicht mit HIV infizierten gesunden erwachsenen Männern ohne hohes HIV-Infektionsrisiko evaluiert.
„Präventive Maßnahmen wie die Präexpositionsprophylaxe könnten eine wichtige Rolle für die Reduktion der Zahl an Neuinfektionen darstellen und dazu beitragen, das Ziel, die globale AIDS-Epidemie zu beenden, zu erreichen“, sagte John C Pottage, Jr, MD, Chief Scientific und Medical Officer, ViiV Healthcare. Die ECLAIR-Ergebnisse wurden im Rahmen der Conference on Retroviruses and Opportunistic Infections (CROI) in Boston (USA) präsentiert.
Cabotegravir – potenzielle Substanz für die HIV-Prävention
Cabotegravir ist ein experimenteller Integrase Strang-Transfer Inhibitor (INSTI) und analog zu Dolutegravir. Cabotegravir wird von ViiV Healthcare zur Behandlung und Prävention von HIV entwickelt und wird derzeit in der Formulierung als sowohl einmal tägliche, orale Tablette als auch lang anhaltende Nanosuspension zur intramuskulären Injektion evaluiert.
Die aktuellen Studiendaten unterstützen die Fortsetzung der klinischen Entwicklung von Cabotegravir – einem sogenannten Integrase Strang-Transfer Inhibitor (INSTI) – als potenzielle Substanz für die HIV-Prävention. Bei 98% der Studienteilnehmer im Cabotegravir-Arm und bei 90% in der Placebogruppe traten während der Injektionsphase unerwünschte Ereignisse auf.
Die ECLAIR-Studie zu Cabotegravir
In der ECLAIR-Studie wurden 127 nicht mit HIV infizierte Teilnehmer im Verhältnis 5:1 in einen Cabotegravir-Arm und eine Placebogruppe randomisiert. Am Beginn des Protokolls stand eine vierwöchige Sicherheits-Beurteilung von oralem Cabotegravir in der Dosierung mit 30mg oder von entsprechenden Placebo-Tabletten.
Gefolgt wurde diese Phase von drei intramuskulären Injektionen von 800 mg Cabotegravir oder Placebo in Form einer sterilen Kochsalzlösung, die in Abständen von jeweils 12 Wochen verabreicht wurden.
Über die ECLAIR-Studie
Bei ECLAIR (Phase IIa Study to Evaluate the Safety, Tolerability and Acceptability of Long Acting Injections of the HIV Integrase Inhibitor [cabotegravir] in HIV Uninfected Men) handelt es sich um eine doppelblinde, randomisierte, multizentrische US-Studie an nicht HIV-infizierten gesunden erwachsenen Männern, die kein hohes HIV-Infektionsrisiko aufweisen. In ECLAIR werden Injektionen von lang wirksamem Cabotegravir als Kandidat für die HIV-Präexpositionsprophylaxe evaluiert.
Die Mehrheit der Studienteilnehmer zeigten sich mit den Cabotegravir-Injektionen zufrieden. Nach wiederholten Injektionen gaben 67 von 91 (74%) der Probanden den lang wirksamen Cabotegravir-Injektionen den Vorzug gegenüber der oralen Cabotegravir-Formulierung.
Diese ersten Resultate der ECLAIR-Studie bestätigen den Forschern das Potenzial von Cabotegravir. Noch in diesem Jahr soll eine Phase III-Studie gestartet werden, um ein noch besseres Verständnis hinsichtlich potenzieller Wirksamkeit und dem Sicherheitsprofil von Cabotegravir in der Präexpositionsprophylaxe zu erhalten.
In der ECLAIR-Studie wurden darüber hinaus Cabotegravir Expositionsdaten über jedes der 12-wöchigen Dosierungsintervalle erhoben. Die Ergebnisse zeigten, dass bei etwa zwei Drittel der Probanden die Substanzkonzentrationen am Ende des Dosierungsintervalls niedriger als erwartet waren.
Als Reaktion auf dieses Resultat wird nun eine alternative Dosierungs-Strategie, bei der 600mg Cabotegravir intramuskulär alle acht Wochen injiziert wird, geprüft. Ziel ist es, die Cabotegravir-Dosierung noch vor Beginn zukünftiger Wirksamkeits- und Sicherheitsstudien zu optimieren.
Nebenwirkungen von Cabotegravir in der ECLAIR-Studie
Bei sieben von 105 Patienten kam es aufgrund von Nebenwirkungen während der oralen Phase zu einem Studienabbruch: drei Fälle von Neutropenie, drei Fälle von erhöhter Creatinphosphokinase (CPK) im Blut und ein Fall von Fatigue.
Von den Studienteilnehmern, die die Injektionsphase erreichten, beendete ein vergleichbarer Anteil in beiden Armen alle drei Injektionszyklen: 93% (87 von 94 Probanden) im Cabotegravir-Arm und 95% (20 von 21 Probanden) in der Placebogruppe.
Von den Probanden selbst berichtete Unverträglichkeit der Injektion führte bei 4% (4 von 94) im Cabotegravir-Arm zum Abbruch. Ein Studienteilnehmer aus der Placebogruppe trat während der Injektionsphase aufgrund einer HIV-Serokonversion zurück.
Weitere Nebenwirkungen während der Injektionsphase im Cabotegravir-Arm – unabhängig von Schmerzen an der Einstichstelle – waren Fieber (Pyrexie), Pruritus (Juckreiz) an der Einstichstelle sowie Schwellung an der Einstichstelle.
Über HIV und einer Präexpositionsprophylaxe
Das Akronym HIV steht für Human Immunodeficiency Virus. Im Gegensatz zu manchen anderen Viren ist der menschliche Organismus nicht in der Lage, diesen Virus zu eliminieren, sodass eine HIV-Infektion lebenslang besteht. Es gibt zwar keine Heilung für HIV, durch effektive Behandlung kann das Virus jedoch so kontrolliert werden, dass Menschen trotz einer HIV-Infektion ein gesundes und erfülltes Leben führen können.
Bei der Präexpositionsprophylaxe (PrEP) handelt es sich um die Anwendung von antiretroviralen Medikamenten durch nicht HIV-infizierte Menschen, vor einer potenziellen Exposition, wodurch einer Infektion mit dem HIV vorgebeugt werden soll.
Aus klinischen Studien zur täglichen oralen Präexpositionsprophylaxe bei nicht HIV-infizierten Personen liegt hochgradige Evidenz für deren Effektivität bei Männern die Sex mit Männern haben (MSM) und gemischtgradige Evidenz für deren Effektivität bei Frauen vor. Derzeit sind zwei Regime zugelassen: eine Fixdosis-Kombination von Tenofovirdisoproxilfumarat (TDF) sowie Emtricatibin (FTC) und TDF alleine.
Quellen und weitere Informationen:
Markowitz M et al. ECLAIR: Phase 2A Safety and PK Study of Cabotegravir LA in HIV Uninfected Men. Presented at the Conference on Retroviruses and Opportunistic Infections (CROI) in Boston, 22-25 February, 2016. Abstract #106
Murray Miranda et al. Tolerability and Acceptability of Cabotegravir LA Injection-results from ECLAIR Study. Presented at the Conference on Retroviruses and Opportunistic Infections (CROI) in Boston, 22-25 February, 2016. Abstract #471
World Health Organization (WHO). Guideline on when to start antiretroviral therapy and on pre-exposure prophylaxis for HIV. September 2015. Last accessed December 2015
http://apps.who.int/iris/bitstream/10665/186275/1/9789241509565_eng.pdf?ua=1
World Health Organization (WHO). Consolidated guidelines on the use of antiretroviral drugs for treating and preventing HIV infection: What’s new. November 2015. Last accessed December 2015
http://apps.who.int/iris/bitstream/10665/198064/1/9789241509893_eng.pdf?ua=1
https://aidsinfo.nih.gov/drugs/513/cabotegravir/0/patient
www.viivhealthcare.com