Die fokal-segmentale Glomerulosklerose (FSGS) ist eine schwerwiegende Nierenerkrankung des Jugend- und Erwachsenenalters.
Fokal-segmentale Glomerulosklerose zeichnet sich durch einen starken renalen Eiweißverlust (Proteinurie) aus und führt unbehandelt rasch zu einem Funktionsverlust der Niere, die eine Nierenersatztherapie notwendig macht und die Lebenserwartung verkürzt. Mutationen in verschiedenen Nierengenen konnten als Ursachen für FSGS identifiziert werden, darunter auch Mutationen in dem Calciumkanal TRPC6. Die allgemein akzeptierte Vorstellung geht davon aus, dass es durch die Genmutationen zu einer Überfunktion von TRPC6 infolge einer Calciumkanal-Aktivierung kommt (sogenannte gain-of-function-Mutationen).
Zusammenhang genetisch unterschiedlicher TRPC6 Mutationen und Fokal-segmentale Glomerulosklerose entdeckt
Ein interdisziplinäres Forscherteam um den Pharmakologen Prof. Christian Harteneck (✝), Universitätsklinikum Tübingen, der Kindernephrologin Prof. Stefanie Weber, Universität Essen (jetzt Marburg), dem Nephrologen Prof. Maik Gollasch, Charité und Max Delbrück Centrum Berlin-Buch, sowie Kooperationspartner aus London, Heidelberg, Hannover, Köln, Freising und Weißwasser konnten jetzt in einem translationalen Ansatz den Zusammenhang genetisch unterschiedlicher TRPC6-Mutationen und dem daraus resultierenden Krankheitsbild dieser seltenen aber klinisch bedeutsamen und für den Patienten belastenden Nierenerkrankung aufzeigen.
Abbildungen zu den Ursachen für Fokal-segmentale Glomerulosklerose
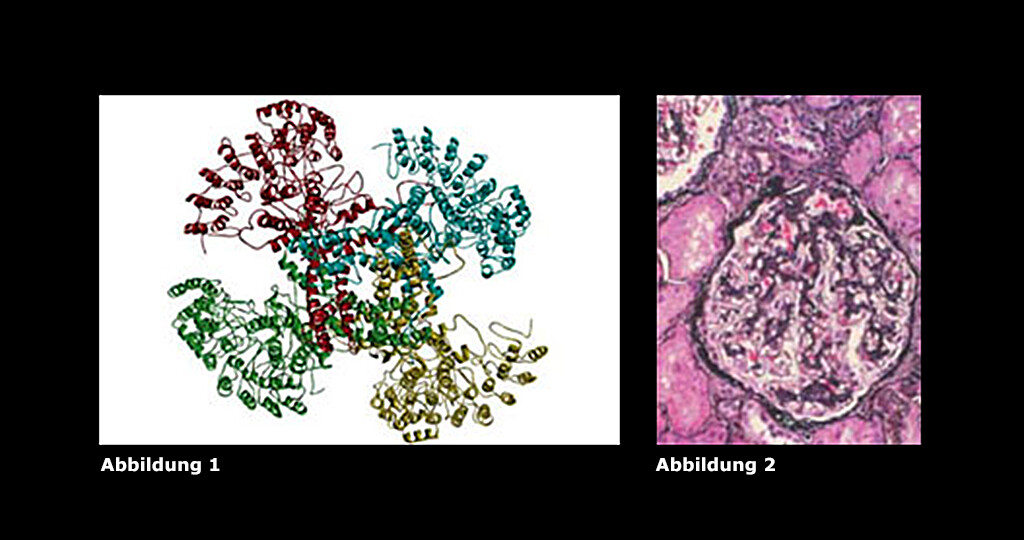
Abb. 1: Ein dreidimensionales in silico-Modell des aus vier Untereinheiten bestehenden TRPC6-Kationenkanals. Dargestellt ist die Ansicht aus extrazellulärer Perspektive. Der Ionenkanalkomplex setzt sich aus vier monomeren TRPC6-Proteinen zusammen, die in unterschiedlichen Farben (rot, hellblau, gelb und grün) dargestellt sind. In der Mitte bilden die vier Monomere eine deutlich sichtbare Ionenkanalpore. (Quelle Riehle et al., JASN, 2016)
Abb. 2: Lichtmikroskopische Aufnahme einer Jones-Methylamin-gefärbten Nierenbiopsie eines Patienten mit einer loss-of-function-TRPC6-Genmutation, der unter einer FSGS Nierenerkrankung leidet. (Quelle Riehle et al., JASN, 2016)
In ihren Untersuchungen weisen sie erstmals nach, dass nicht nur gain-of-function- sondern auch loss-of-function-Mutationen bei betroffenen Patienten zu FSGS führen. Letztere neu entdeckte Genveränderungen bewirken eine Inaktivierung des TRPC6-Ionenkanals mit der Folge einer verminderten Calciumkanalaktivität, die als loss-of-function bezeichnet wird. Diese unerwarteten Befunde erweitern das Verständnis zu den pathogenen Konsequenzen einer genetisch veränderten TRPC6 Kanalaktivität im Menschen. Sie bedeuten, dass sowohl ein erhöhter als auch ein verminderter Calciumeinstrom über TRPC6 in spezialisierte Nierenzellen, den sogenannten Podozyten, zu ein und derselben Nierenerkrankung (FSGS) führen können. Dreidimensionale Strukturanalysen an Modellen der krankhaft veränderten Kanalproteine belegen zudem, dass räumliche (sterische) Veränderungen in den Proteinen die beobachteten Funktionsveränderungen bewirken. Die gegenwärtigen Arbeiten konzentrieren sich nun auf pharmakologische Eingriffsmöglichkeiten, um die Fehlfunktion der mutierten TRPC6-Kanäle zu korrigieren.
Die Ergebnisse dieser neuen Studie zeigen in besonderer Weise auf, wie wichtig die enge wissenschaftliche Kooperation zwischen Vertretern von experimentell-zellbiologischer Forschung auf der einen und klinisch-wissenschaftlicher Arbeit auf der anderen Seite ist.
Publikation
TRPC6 G757D Loss-of-Function Mutation Associates with FSGS
Marc Riehle, Anja K. Büscher, Björn-Oliver Gohlke, Mario Kaßmann, Maria Kolatsi-Joannou, Jan H. Bräsen, Mato Nagel, Jan U. Becker, Paul Winyard, Peter F. Hoyer, Robert Preissner, Dietmar Krautwurst, Maik Gollasch, Stefanie Weber, and Christian Harteneck
JASN September 2016 27: 2771-2783; published ahead of print February 18, 2016, doi:10.1681/ASN.2015030318
http://jasn.asnjournals.org/content/27/9/2771.abstract