Pathophysiologie im Blickpunkt: Ursachen und Entstehung der Multiplen Sklerose (MS), Mechanismen der Gewebeschädigung und Reparaturmechanismen.
Weltweit sind über eine Million Menschen an Multipler Sklerose (MS) erkrankt, der häufigsten neurologischen Erkrankung bei jungen Erwachsenen. Ein chronisch entzündlicher Prozess im zentralen Nervensystem (ZNS) führt bei dieser Erkrankung zur Zerstörung der Markscheiden und im weiteren Verlauf auch der Axone. Dadurch entstehen die für die MS typischen großen Entmarkungsherde im zentralen Nervensystem. Entstehung und Ursache der Multiplen Sklerose sind bislang nicht völlig geklärt, doch muss – entsprechend dem derzeitigen Wissensstand – eine autoimmunologische Genese, bei der eine genetische Disposition und Umweltfaktoren eine Rolle spielen, als sehr wahrscheinlich angenommen werden.
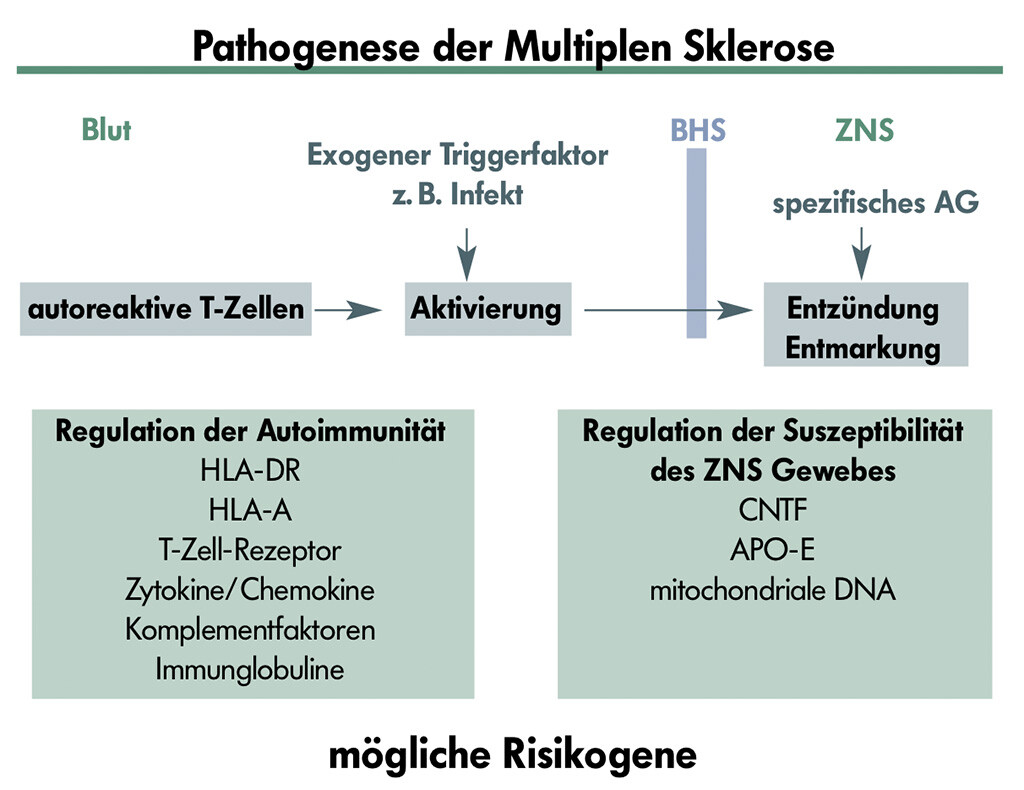
Autoreaktive T-Lymphozyten, die auch beim gesunden Menschen Bestandteil des Immunsystems sind, nehmen eine Schlüsselrolle als primäre Auslöser der Krankheit ein. Um das systemische Immunkompartment verlassen –, und durch Überwindung der Blut-Hirn-Schranke – in das ZNS gelangen – zu können, müssen diese Zellen durch einen exogenen Faktor (z.B. durch einen Infekt) aktiviert werden. Wenn diese peripher aktivierten T-Lymphozyten ihr spezifisches Antigen im ZNS vorfinden, und dieses zusammen mit HLA-Molekülen und weiteren Signalen von Makrophagen präsentiert wird, beginnt die entzündliche Reaktion.
Eine entscheidende Rolle bei den nachfolgenden Ereignissen spielen verschiedene Botenstoffe des Immunsystems (Zytokine, Chemokine), welche von hämatogenen und lokalen Zellen des ZNS gebildet werden. Diese Botenstoffe bewirken z.B. die Aufregulierung von Molekülen an der Blut-Hirn-Schranke, welche die Adhäsion von Zellen erleichtern, wodurch weitere, nicht aktivierte Entzündungszellen an den Ort der Entzündung gelangen können.
Eine genetische Disposition, die die Entstehung einer Autoimmunerkrankung begünstigt oder das ZNS Gewebe empfindlicher für »Attacken« des Immunsystems macht, spielt bei der Auslösung der Multiplen Sklerose eine wichtige Rolle. Nach jüngstem Wissensstand besteht ein Zusammenhang zwischen bestimmtem genetischen Defekten und schwererer Erkrankung.
Im Tiermodell der MS zeigen Tiere, denen das CNTF (ciliärer neurotropher Faktor)-Gen fehlt, ein vorzeitiges Sterben der Stammzellen der Oligodendrozyten (= Markscheiden-bildende Zellen), sowie einen früheren Erkrankungsbeginn und progredienten Verlauf. Ebenso erkranken MS Patienten mit einem genetisch inaktiven CNTF früher und schwerer. Rezente kernspintomographische Erkenntnisse belegen eine ausgeprägtere Gewebezerstörung bei MS Patienten mit dem ApoE-epsilon4 Allel.
Viele Wege führen zur Entmarkung
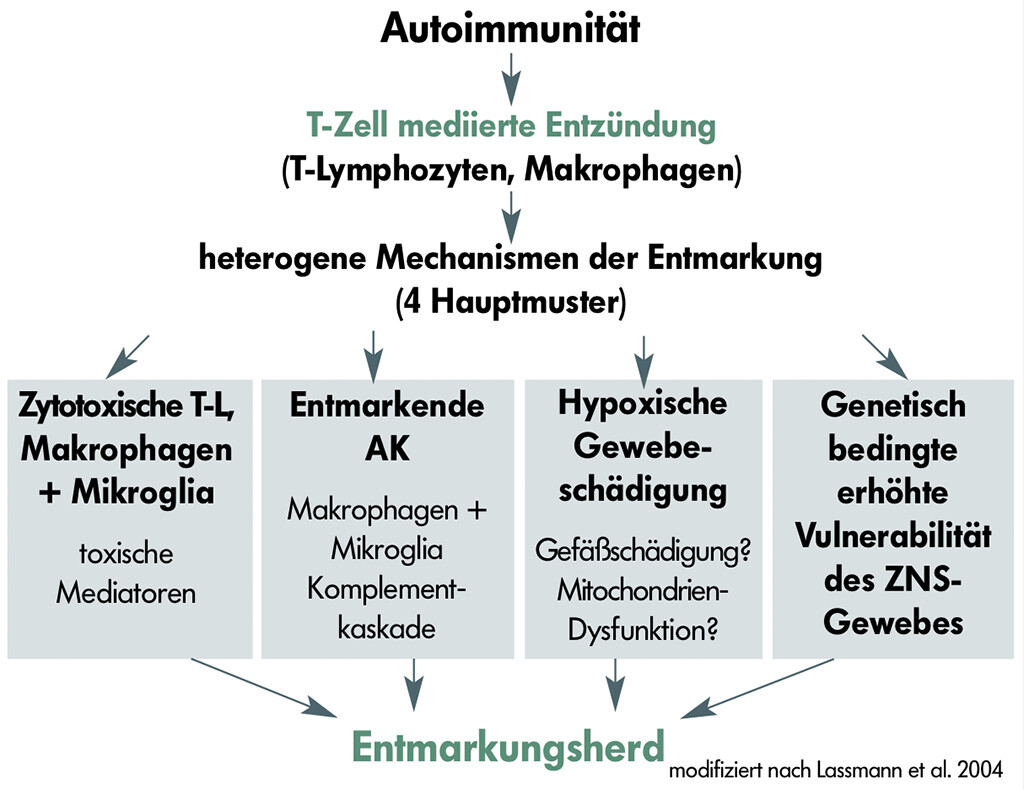
Ein wesentlicher Erfolg der MS Forschung der letzten Jahre ist die Erkenntnis, dass die Zerstörung der Markscheiden keine einheitliche Ursache hat. Im Verlauf der von T-Lymphozyten gesteuerten entzündlichen Reaktion, können verschiedene Mechanismen zur Entstehung der charakteristischen Entmarkungsherde führen. Diese unterschiedlichen pathogenetischen Mechanismen führen zu unterschiedlichen neuropathologischen Veränderungen. Prof. Hans Lassmann und Mitarbeiter (Zentrum für Hirnforschung, Medizinische Universität Wien) konnten vier unterschiedliche Muster von pathologischen Veränderungen in aktiven Multiple Sklerose-Herden differenzieren. Diese Entmarkungsmuster sind unterschiedlich bei verschiedenen MS-Patienten, jedoch homogen in ein und demselben Patienten.
Die Unterscheidung dieser verschiedenen pathologischen Subtypen mittels paraklinischer Marker (Kernspintomographie, Liquoranalysen, Genotypisierung) stellt ein zentrales Anliegen gegenwärtiger Multiple Sklerose Forschung dar. Eine Gemeinsamkeit aller vier Muster ist die entzündliche Reaktion, welche hauptsächlich aus T-Lymphozyten und Makrophagen besteht (Entmarkungsmuster I-IV).
Entmarkungsmuster I.
Das Entmarkungsmuster I besteht ausschließlich aus der entzündlichen Reaktion. Toxische Substanzen aus zytotoxischen T-Lymphozyten und Makrophagen verursachen die Zerstörung der Markscheiden.
Entmarkungsmuster II.
Beim Entmarkungsmuster II kommt es zusätzlich zu den T-Lymphozyten und Makrophagen in Arealen mit aktiver Markscheidenzerstörung, zu Ablagerungen von Antikörpern und Komplementfaktoren an zugrundegehenden Oligodendrozyten und Markscheiden. Auf der Basis einer T-Lymphozyten-mediierten Entzündung führen bei diesem Muster entmarkende Antikörper zum Markscheidenuntergang.
Entmarkungsmuster III.
Das Entmarkungsmuster III ist charakterisiert durch den Verlust von bestimmten Markscheidenproteinen, wohingegen andere Markscheidenproteine kaum oder nicht betroffen sind. Ein weiteres Merkmal sind apoptotische Oligodendrozyten, woraus geschlossen werden kann, dass die Oligodendrozyten das primäre Angriffsziel der Zerstörung sind und die Markscheiden konsekutiv zugrunde gehen. Als diesem Muster zugrundeliegender pathogenetischer Mechanismus wird eine hypoxische Gewebszerstörung angenommen, da ebensolche Veränderungen auch bei der akuten Ischämie der weißen Substanz vorkommen.
Entmarkungsmusters IV.
Das herausragende Merkmal des Entmarkungsmusters IV ist die primäre Degeneration von Oligodendrozyten. Oligodendrozyten und Markscheiden werden nahezu vollständig zerstört und Remyelinisierungsvorgänge fehlen. Die genauen, diesem Entmarkungsmuster zugrunde liegenden Mechanismen sind derzeit noch nicht bekannt. Genetisch bedingte Veränderungen könnten die Oligodendrozyten empfindlicher für immun-mediierte Zerstörung machen.
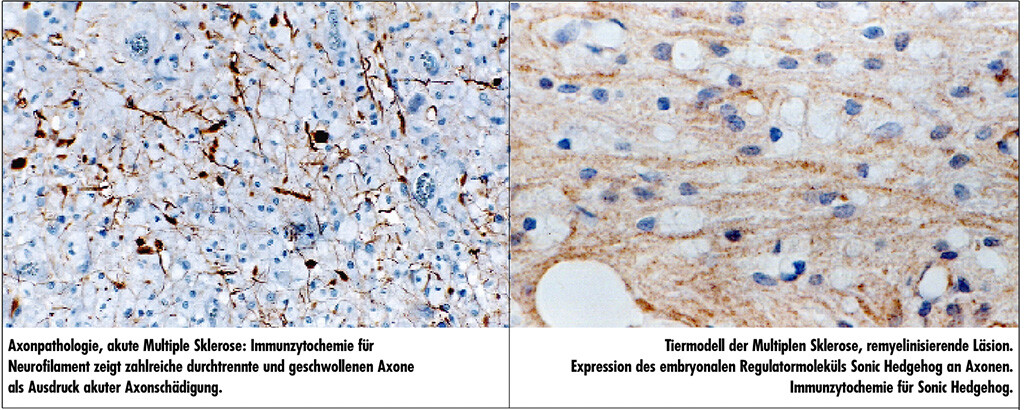
Axonschädigung
Der chronisch entzündliche Entmarkungsprozess führt primär zu einer Zerstörung der Markscheiden, jedoch werden die Axone im weiteren Verlauf des Entmarkungsprozesses ebenfalls geschädigt. Nach Überschreiten einer kritischen Schwelle ist die Axonschädigung irreversibel. Das Ausmaß des Axonschadens korreliert mit den bleibenden neurologischen Ausfällen und variiert sehr stark zwischen den einzelnen Multiple Sklerose – Patienten. Am ausgeprägtesten ist die Axonzerstörung in der akuten Multiplen Sklerose, sowie in aktiv entmarkenden Herden. Aber auch in chronischen Läsionen schreitet der Prozess der Axonschädigung kontinuierlich fort, wodurch die klinische Progredienz der Erkrankung bei Fehlen von Aktivitätszeichen erklärt werden kann.
Die genauen molekularen Mechanismen der Axonschädigung sind derzeit noch unbekannt, doch großteils dürften toxische Substanzen, welche aus den Entzündungszellen freigesetzt werden, für die Entstehung des Axonschadens verantwortlich sein. Die Störung des Ionenkanalsystems durch diese entzündlichen Mediatoren führt in weiterer Folge zur Akkumulation von intrazellulärem Kalzium mit konsekutiver Aktivierung von Enzymen und dem Abbau des Zytoskelettes. Die dadurch hervorgerufene Störung des axonalen Transportes führt zur Ausbildung eines (reversiblen) Leitungsblocks. Bei Fortbestehen der schädigenden Einflüsse entsteht durch Durchtrennung der Axone mit Degeneration der distalen Anteile ein irreversibler Axonverlust. In chronisch inaktiven Herden dürfte einem Mangel an trophischen Faktoren eine entscheidende Rolle beim Fortschreiten des Axonschadens zukommen.
Reparaturmöglichkeiten
Durch Remyelinisierung werden demyelinisierte Herde »repariert«: Axone werden durch Wiederumscheidung mit Markscheiden vor Schädigung durch toxische Substanzen geschützt und eine sichere Nervenleitung wird nach einem Leitungsblock wiederhergestellt. Insbesondere im Frühstadium des Krankheitsverlaufes können entmarkte Herde durch Remyelinisierung repariert werden. In späten Stadien der chronischen MS fehlen remyelinisierte Herde meist völlig oder sind auf schmale Areale, die den entmarkten Herd umgeben, beschränkt.
Generell weisen Entmarkungsherde, in denen viele Oligodendrozyten vorhanden sind, eine Remyelinisierung auf. Der Verlust von Oligodendrozyten in den Entmarkungsherden ist durch geringe oder fehlende Remyelinisierung gekennzeichnet. Remyelinisierende Oligodendrozyten stammen in erster Linie von undifferenzierten Stammzellen ab. Oligodendrozyten, welche in den entmarkten Arealen überlebt haben, könnten jedoch auch eine Rolle bei Reparationsvorgängen spielen.
Neben der Anzahl der zur Verfügung stehenden Markscheiden-bildenden Zellen und dem Ausmaß des Axonschadens, beeinflussen noch weitere Faktoren, wie das Ausmaß der gliösen Narbenbildung und das Vorhandensein von Wachstumsfaktoren im Entmarkungsherd, eine erfolgreiche Remyelinisierung.
Rezente Studien belegen, dass ausreichend Oligodendrozyten-Stammzellen in chronischen MS Läsionen vorhanden sind, diese jedoch nicht in der Lage sind, die entmarkten Axone mit ihren Fortsätzen wieder zu umscheiden. Dieses Unvermögen zu remyelinisieren dürfte auf fehlende »Signale« aus der Umgebung der Oligodendrozyten-Stammzellen zurückzuführen sein.
Entstehung und Ursache der Multiplen Sklerose sind nicht geklärt, man vermutet, dass genetische Disposition und Umweltfaktoren sehr wahrscheinlich eine Rolle spielen.
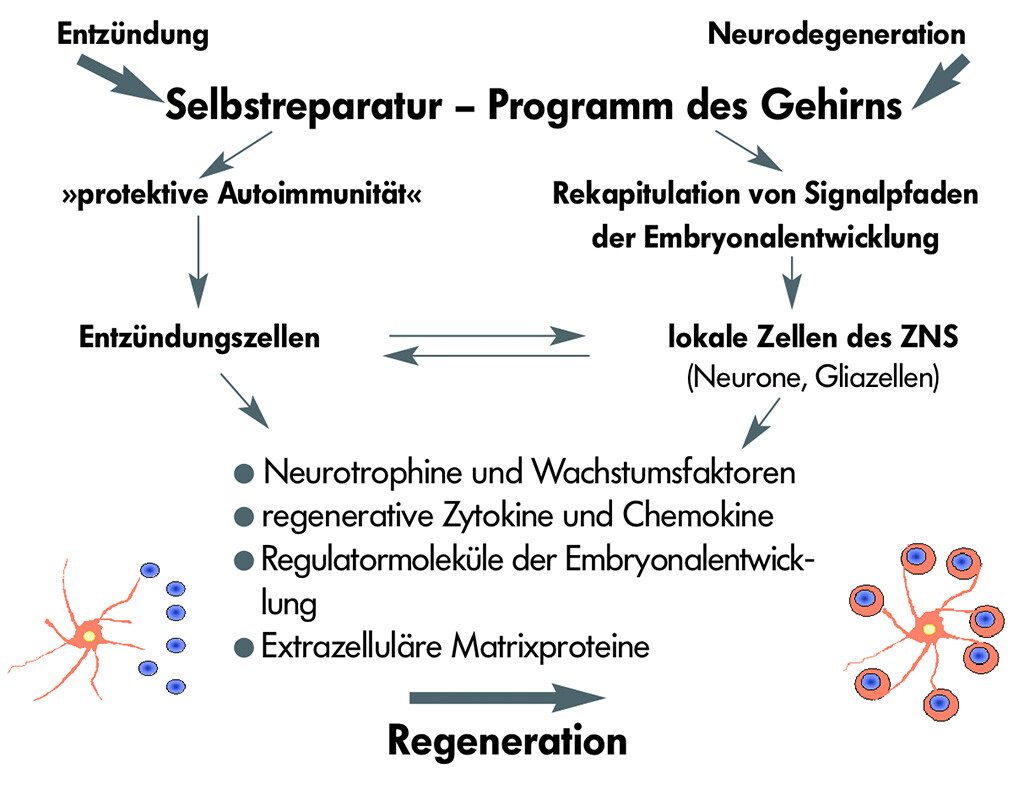
Als Antwort auf Entzündung oder Neurodegeneration löst der Organismus ein »Selbstreparaturprogramm« des Gehirns aus. Dieses induziert zwei Systeme: Die sogenannte »protektive Autoimmunität« und das Wiederauftreten von regenerativen Molekülen, die in der Entwicklung des ZNS eine Rolle spielen.
Die »protektive Autoimmunität« ist sozusagen die »gute Seite« der Entzündung und befindet sich mit »der schlechten Seite«, die für die Gewebszerstörung verantwortlich ist, in einem sensiblen Gleichgewicht. Aktuelle Untersuchungen zeigen, dass aktivierte T-Zellen und andere Entzündungszellen in MS Läsionen neuroprotektive Faktoren, wie beispielsweise BDNF, produzieren (brain derived neurotrophic factor), welche das Überleben von Neuronen und Axonen, sowie die Proliferation von Oligodendrozyten fördern. Diese duale Rolle der Entzündung kann auch die unbefriedigenden Behandlungserfolge mit nicht selektiven Immunsuppressiva in der Langzeittherapie der Multiplen Sklerose erklären.
Moleküle, die in der Embryonalzeit die Ausbildung von ZNS Strukturen regulieren und steuern und normalerweise im gesunden Gehirngewebe nach der Geburt nicht mehr vorhanden sind, können unter pathologischen Bedingungen wieder neu gebildet werden und zur Regeneration beitragen. So wurden kürzlich Faktoren gefunden, die bei der Entwicklung der Oligodendrozyten und Axone eine Rolle spielen. Sowohl in remyelinisierenden Herden der MS als auch in denen des Tiermodells.
Durch die Aktivierung des Reparaturprogrammes setzen Entzündungszellen und lokale Zellen des ZNS Wachstums- und Überlebensfaktoren frei, welche die Regeneration fördern. Darüber hinaus hat das Reparaturprogramm des ZNS auch immunmodulierende Funktionen, wie die Hemmung der Aufregulierung von HLA-Molekülen.
Im Verlauf chronisch entzündlicher oder chronisch degenerativer Erkrankungen erschöpft sich offenbar die Reparaturkapazität des ZNS. Um therapeutische Strategien zur exogenen Stimulierung dieser Reparaturmechanismen zu entwickeln, wird die weitere Erforschung der genauen molekularen Mechanismen der regenerativen Prozesse des ZNS nötig sein.
Literatur:
Compston A, Coles A. Multiple sclerosis. Lancet. 2008;372(9648):1502‐1517. doi:10.1016/S0140-6736(08)61620-7
Anagnostouli M, Markoglou N, Chrousos G. Psycho-neuro-endocrino-immunologic issues in multiple sclerosis. A critical review of clinical and therapeutic implications [published online ahead of print, 2020 Jun 1]. Hormones (Athens). 2020;10.1007/s42000-020-00197-8. doi:10.1007/s42000-020-00197-8
Multiple sclerosis. Nat Rev Dis Primers. 2018;4(1):44. Published 2018 Nov 8. doi:10.1038/s41572-018-0046-z
Quellen:
Entstehung der Multiplen Sklerose. Univ.-Prof. Dr. Maria Storch, Prof. Helene Breitschopf. MEDMIX 07–08/2005, S15–18.
http://www.awmf.org/leitlinien/detail/ll/030-050.html
http://www.dmsg.de/multiple-sklerose-news/index.php?w3pid=news&kategorie=forschung&anr=5552