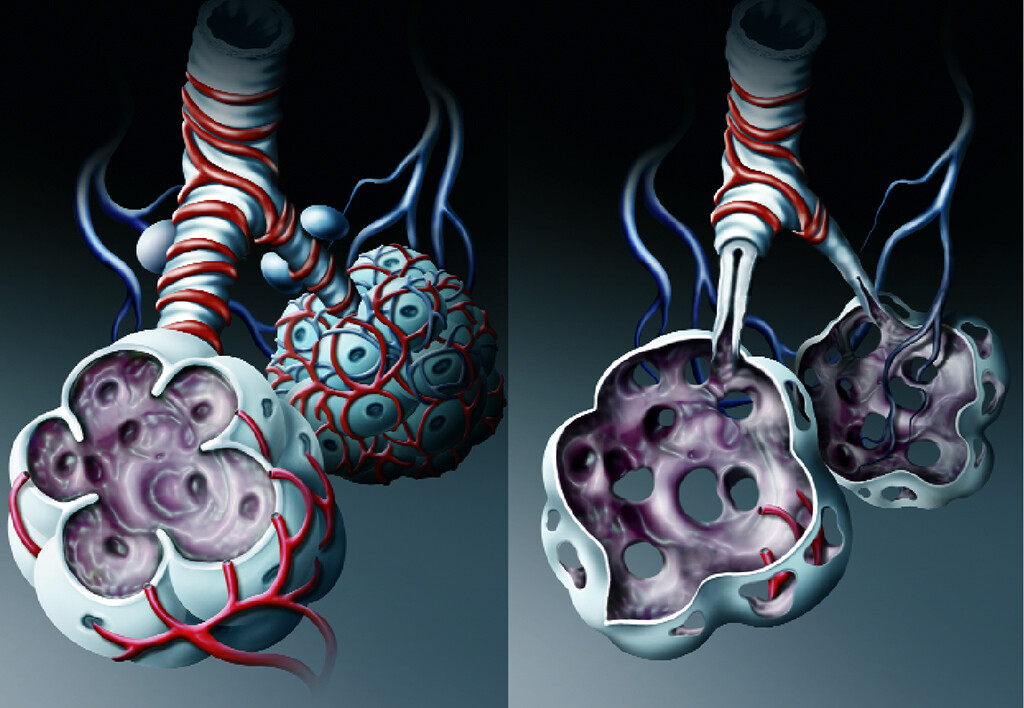
Die Diagnose COPD basiert auf einer Atemflussbehinderung. Die Therapie zielt darauf ab, die fortschreitende Parenchymzerstörung der Lunge zu verhindern.
Da bei chronisch obstruktiven Krankheiten der Lunge – der COPD – das Symptom der Atemnot klinisch erst zu einem Zeitpunkt manifest wird, wenn bereits eine hochgradige Atemstrombehinderung besteht, ist ein Screening mittels kleiner Spirometrie bei Hochrisikogruppen (Raucher über 40 Jahre, Husten, Sputumproduktion, Familienanamnese) angezeigt. Die Therapie der COPD sollte zu einem frühen Zeitpunkt beginnen – das gilt folglich auch für die frühe Diagnose COPD – und darauf abzielen, die progrediente Parenchymzerstörung der Lunge zu verhindern. Meist stellt dabei die Nikotinkarenz die effektivste präventive Maßnahme dar, gefolgt von einer Minimierung der bronchialen Obstruktion.
Entzündung der kleinen Luftwege führt zu Atemflussbehinderung
»Chronic Obstructive Pulmonary Disease – COPD« ist eine Erkrankung, die durch eine nicht vollständig reversible Atemflussbehinderung charakterisiert ist. Diese ist progressiv und mit einer abnormen inflammatorischen Antwort der Lunge auf schädigende Partikel und Gase verbunden.
Die Atemflussbehinderung ist das Resultat einer Entzündung der kleinen Luftwege (obstruktive Bronchiolitis) und einer Lungenparenchymdestruktion (Emphysem). Der relative Anteil dieser beiden Komponenten ist von Patient zu Patient unterschiedlich, wobei zusätzlich eine Überempfindlichkeit der Atemwege (Hyperreaktivität) bestehen kann.
Klinisch bestehen Husten, vermehrte Schleimproduktion, Atemnot und exspiratorische Atemstrombehinderung. Fast alle Patienten mit COPD sind Raucher. Im Gegensatz zum »Asthma bronchiale«, bei der die Atemstrombehinderung meist spontan reversibel ist, zeigt die exspiratorische Atemstrombehinderung bei der COPD – abgesehen von Infektexazerbationen – keine wesentliche spontane Variabilität.
Diagnose COPD sehr selten in frühen Stadien der Erkrankung der Lunge
Obwohl der Arzt die chronisch obstruktive Lungenkrankheit (COPD) formal mittels Spirometrie diagnostiziert und quantifiziert, erfolgt die Verdachts-Diagnose dieser Erkrankung der Lunge meist klinisch. Da sich Symptome wie Husten, Sputumproduktion und Atemnot erst in einem späteren Stadium der Erkrankung manifestieren und die Erkrankungen einen langsam progredienten Verlauf aufweist, wird die Diagnose COPD sehr selten in frühen Stadien gestellt.
Der typische Patient mit COPD ist über 40 Jahre alt und hat mehr als 20 Pack/years geraucht (1 Pack/year entspricht 20 Zigaretten/Tag über 1 Jahr). Jene Patienten, die weniger geraucht haben und die klinischen Zeichen einer COPD aufweisen, sollten auf einen Alpha-1-Antitrypsinmangel und/oder Asthma bronchiale näher untersucht werden. Üblicherweise suchen COPD-Patienten aufgrund eines chronischen Hustens und/oder produktiven Sputums den Arzt auf. Später tritt Atemnot bei Belastung und schließlich in Ruhe auf.
Husten häufigstes Symptom von Patienten mit COPD
Intermittierender oder persistierender chronischer Husten mit oder ohne Sputumproduktion ist das häufigste Symptom von Patienten mit COPD. Husten tritt üblicherweise am frühen Morgen, vor allem im Winter auf. Die meisten Patienten ignorieren diese Symptome, da offensichtlich keine Einschränkung der Lebensqualität verursacht ist (Raucherhusten). Später tritt der Husten nicht nur morgens, sondern während des ganzen Tages und während des gesamten Jahres auf. Die Sputumproduktion ist meist mukoid, kann sich allerdings auch gelblich verfärben (vor allem während akuter Exacerbationen).
Atemnot wird zunächst während Belastung (Stiegen steigen) und während akuten bronchialen Exacerbationen festgestellt. Das Auftreten von Atemnot bedeutet bereits eine weit fortgeschrittene Einschränkung der Lungenfunktion mit einer Einsekundenkapazität (FEV1) meist unter 50% des individuellen Sollwertes. Das subjekive Empfinden der Atemnot korreliert dabei schlecht mit objektiven Lungenfunktionsparametern.
Grad der Atemnot quantifizieren
Gemäß der MRC (Medical Research Council)-Klassifikation kann der Arzt das Grad der Atemnot wie folgt quantifizieren. Hämoptysen treten gelegentlich, vor allem während akuten Exacerbationen auf, wobei andere Ursachen wie Lungenkrebs und Bronchiektasien ausgeschlossen werden müssen. Die meisten Episoden von Hämoptyse bei COPD sind allerdings durch Entzündung der Bronchialschleimhaut und nicht durch Lungenkrebs oder Bronchiektasien bedingt. Gewichtsverlust und Anorexie sind Symptome in späten Stadien der COPD, deren Ursache weiterhin ungeklärt ist.
Man geht heute davon aus, dass die COPD eine systemische Erkrankung ist, die durch generalisierte Muskelschwäche und Gewichtsverlust charakterisiert ist. In wie weit TNF-Alpha hierbei eine kausale Rolle spielt ist Gegenstand rezenter Forschung.
Diagnose COPD – Lungenfunktion und arterielle Blutgasanalyse
Die Diagnose COPD basiert auf einer Atemflussbehinderung der Lunge. Der Nachweis kann mittels Spirometrie, Fluss-Volumen-Kurve oder Ganzkörperplethysmographie erfolgen. In allen Verdachtsfällen und bei allen Schweregraden der COPD sowie zur Differentialdiagnose der Dyspnoe sollte eine Lungenfunktionsprüfung durchgeführt werden. Erkrankungen, die differntialdiagnostisch ausgeschlossen werden müssen, sind in erster Linie Asthma bronchiale, Bronchiektasien, restriktive Ventilationsstörungen, Lungenkrebs, Linksherzversagen, die venöse Thromboembolie (Pumonalembolie) und schwere Anämien.
Die Spirometrie mit der Messung der langsamen (VC) und forcierten in- und exspiratorischen Vitalkapazität (FVC), und der Einsekundenkapazität (FEV1) stellt die Basis der objektiven Darstellung der Atemflussbehinderung dar. Die Messung der Einsekundenkapazität (FEV1) ist zudem entscheidend, den Schweregrad der Erkrankung zu definieren (siehe später). Sie ist auch in der Lage, die Prognose des Patienten abzuschätzen und eignet sich in Longitudinaluntersuchungen, die Progression der Erkrankung zu dokumentieren.
Messung der FEV1
Die Messung der FEV1 ist einfach und weist eine geringe Inter- und Intraobserver-Variabilität auf. Zudem gibt es für die FEV1 die am besten definierten Normalwerte bezogen auf Alter, Rasse, Geschlecht und Größe. Gemäß der globalen Initiative für chronisch obstruktive Lungenerkrankungen (GOLD), eine von der Weltgesundheits- Organisation (WHO), dem National Institut of Health (NIH) und dem National Heart, Lung und Blood Institut (NHLBI) gemeinsam 2003 erarbeiteten Richtlinien über Diagnose und Behandlung der COPD, definieren 4 Schweregrade der COPD. Diese Schweregrade haben wesentliche Implikationen auf die einzuschlagende Therapie.
Eine Atemflussbehinderung wird dann diagnostiziert, wenn die Einsekundenkapazität in Relation zur forcierten Vitalkapazität (FVC) vermindert ist (wenn das Verhältnis FEV1/FVC unter 70% fällt). Das Verhältnis FEV1/FVC ist relativ sensitiv bei leichten Formen der COPD, während bei schwerer COPD die VC aufgrund einer Zunahme des RV (dynamische Überblähung) ebenfalls fällt und damit die Sensitivität dieses Verhältnis vermindert.
Diagnose COPD und deren Schweregrade
Der Schweregrad der COPD (entsprechend der GOLD-Kriterien) wird ermittelt anhand der Einsekundenkapazität (FEV1), gemessen nach Inhalation eines Beta 2 Sympatikomimetikums oder Parasympatikolytikums, im Verhältnis zum individuellen Sollwert.
Etwa 20% der Patienten mit COPD zeigen einen Anstieg des FEV1 um 15% nach Inhalation eines Beta 2 Sympatikomimetikums oder Parasympatikolytikums. Eine derartige Obstruktion wird demnach als partiell reversibel eingestuft. Überlicherweise verbessern sich COPD-Patienten nicht akut, sondern erst nach längerer bronchospasmolytischer Therapie.
Verschiedene andere Indizes – maximaler exspiratorischer Fluss bei 75%, 50% und 25% der Vitalkapazität; MEF 75%, MEF 50%, MEF 25% – können während einer forcierten Exspiration durch Darstellung der Fluss-Volumen-Kurve erhoben werden. Die Kalkulation jener Indizes, die man in der Fluss-Volumen-Kurve darstellen kann, und die mit den heutigen automatischen Spirometern ausgeworfen sind, sind allerdings von geringerer Bedeutung als VC und FEV1.
Vor allem der MEF 25% soll die bronchiale Obstruktion der kleinen Luftwege repräsentieren. Die Messung des exspiratorischen Peak-flows (PEF) ist für die Erstdiagnose nicht zu empfehlen, eignet sich jedoch für das Monitoring der Lungenfunktion zu Hause, am Arbeitsplatz und vor allem für die Feststellung der täglichen Schwankungen, die allerdings bei Asthma bronchiale wesentlich ausgeprägter ausfallen, als bei Patienten mit COPD.
Hypoxämie und Hyperkapnie
Die Bodypletysmographie ist dem Facharzt für Lungenkrankheiten, dem Labor im Spital sowie Schwerpunktkrankenhäusern vorbehalten. Bei milden Formen der COPD können PaO2 und PaCO2 normal sein. Bei Fortschreiten der Erkrankung allerdings findet man häufig eine Hypoxämie und eine Hyperkapnie.
Eine Hyperkapnie findet sich meist erst bei einem FEV1 unter 1 l. Hypoxämie und Hyperkapnie verschlechtern sich üblicherweise während akuten Exacerbationen und können auch während Belastung und Schlaf auftreten. Eine Zunahme des Hämatokrits (Erythrozytose) wird selten bei Patienten mit COPD festgestellt. Die Wahrscheinlichkeit erhöht sich ab einem arteriellen O2-Partialdruck unter 55mmHg.
Weitere Maßnahmen zur Diagnose COPD
Die Diagnose COPD wird wie besprochen durch einen Lungenfunktionstest festgestellt beziehungsweise klinisch vermutet. Schließlich dienen weiterführende diagnostische Maßnahmen in erster Linie zur Abgrenzung anderer Lungenerkrankungen. Wichtig ist weiters, dass die Diagnostik auch den Schweregrad der COPD und mögliche Komplikationen feststellt.
Die wesentliche Indikation zu bildgebenden Verfahren ist somit die Diagnose COPD zu erhärten. Schließlich sind auch differenzialdiagnostisch andere Erkrankungen, die ähnliche klinische Zeichen und Symptome zeigen (Bronchiektasien, Lungenkrebs, etc.), auszuschließen.
Neue bildgebende Verfahren (HR-CT) erlauben es zunehmend, den Schweregrad der Erkrankung bildgebend darzustellen und zwischen unterschiedlichen Formen des Emphysems (zentrilobulär, panazinär) zu unterscheiden. Das Elektrocardigramm liefert Informationen über das Vorliegen einer koronaren Herzkrankheit, Linksherzhypertrophie oder über Herzrythmusstörungen, ist jedoch eine insensitive Methode zur Diagnose einer rechtsventrikulären Hypertrophie (Cor pulmonale).
Eine Abweichung der anatomischen Herzachse nach rechts, ein inkompletter Rechtsschenkelblock, ein P-Pulmonale sowie uncharakteristische ST-Veränderungen in den Ableitung V1 – V3 stellen Hinweise für eine rechtsventrikuläre bzw. rechtsarteriale Hypertrophie dar.
Echocardiographie
Die Echocardiographie ist die mit Abstand beste, nicht invasive Methode, um einen erhöhten Pulmonalarteriendruck abschätzen zu können. Voraussetzung für eine adäquate Messung ist allerdings das Bestehen einer Trikuspidalinsuffizienz, die in Abhängigkeit vom Schweregrad der Grundkrankheit und Auftreten der pulmonalarteriellen Hypertension auftritt.
Gemäß publizierter Studien, kann mit dieser Methode ein erhöhter Druck im kleinen Kreislauf bei etwa 80% der Patienten mit COPD festgestellt werden.
Therapieziele für die Lunge bei Diagnose COPD
Alle Therapiestrategien sollten darauf abzielen, das Fortschreiten der strukturellen Zerstörung von Lungenparenchym zu verhindern. Demnach kommt der Früherkennung einer gestörten Funktion der Lunge und der rechtzeitigen Eliminierung von Risikofaktoren eine zentrale Rolle zu.
Daneben kommt der konsequenten medikamentösen und nicht medikamentösen Therapie in der chronischen Phase der Erkrankung eine wesentliche Rolle zu. Schließlich sollten akute Exazerbationen früh erkannt und entsprechend behandelt werden. Denn sie beeinflussen die Progression der Erkrankung und die Lebensqualität der Patienten sehr negativ.
Prävention der COPD: Raucherentwöhnung
Die von GOLD vorgeschlagenen therapeutischen Maßnahmen richten sich auch nach der Schweregradeinteilung. Die Messung der FEV1 ist einfach und weist eine geringe Inter- und Intraobserver-Variabilität auf.
Neben der festgestellten Einschränkung der Lungenfunktion kann mit der Spirometrie auch durch longitudinale Untersuchungen der jährliche Abfall der Lungenfunktion anhand der Einsekundenkapazität objektiviert werden, der im Vergleich zu lungengesunden Patienten (20-40ml/Jahr) 50-120ml/Jahr beträgt.
Bislang konnte lediglich durch Nikotinkarenz gezeigt werden, dass dieser jährliche Abfall signifikant beeinflusst werden kann. Demnach stellt auch weiterhin die Raucherentwöhnung die effektivste präventive Maßnahme dar, wobei Risikopatienten im vierten Lebensjahrzehnt besonders profitieren.
Durch Nikotinersatztherapie und Medikamente kann das wichtige Aufklärungs- und Informationsgespräch zwischen Arzt und Patient, welches auf das persönliche Risikoprofil eingehen sollte, unterstützt werden. Durch die Kombination all dieser Maßnahmen können wenigstens 10 bis 20% der Raucher langfristig vom Nikotin entwöhnt werden.
Literatur:
Rabe KF, Watz H. Chronic obstructive pulmonary disease. Lancet. 2017 May 13;389(10082):1931-1940. doi: 10.1016/S0140-6736(17)31222-9. Epub 2017 May 11. PMID: 28513453.
Yang IA, Brown JL, George J, Jenkins S, McDonald CF, McDonald VM, Phillips K, Smith BJ, Zwar NA, Dabscheck E. COPD-X Australian and New Zealand guidelines for the diagnosis and management of chronic obstructive pulmonary disease: 2017 update. Med J Aust. 2017 Nov 20;207(10):436-442.
Dheeraj Gupta, Ritesh Agarwal, Ashutosh Nath Aggarwal, V. N. Maturu, Sahajal Dhooria, K. T. Prasad, Inderpaul S. Sehgal, Lakshmikant B. Yenge, Aditya Jindal, Navneet Singh, A. G. Ghoshal,1 G. C. Khilnani,2 J. K. Samaria,1 S. N. Gaur,2 D. Behera, and S. K. Jindal for the COPD Guidelines Working Group. Guidelines for diagnosis and management of chronic obstructive pulmonary disease: Joint ICS/NCCP (I) recommendations. Lung India. 2013 Jul-Sep; 30(3): 228–267. doi: 10.4103/0970-2113.116248
Quellen:
COPD – Eine Herausforderung für die Gesellschaft. Prim. Univ.-Prof. Dr. O.C. Burghuber. MEDMIX 03/2006; S8-14.
Global Initiative for Chronic Obstructive Lung Disease (GOLD)